يظل (MI) السبب الأكثر شيوعًا لمكالمات الطوارئ رعاية طبية(SMP). تعكس ديناميكيات عدد المكالمات في موسكو لـ MI على مدى ثلاث سنوات (الجدول 1.) استقرار عدد مكالمات سيارات الإسعاف لـ MI على مدى ثلاث سنوات وثبات نسبة حالات احتشاء عضلة القلب المعقدة وغير المعقدة. أما بالنسبة لدخول المستشفى ، فقد ظل العدد الإجمالي عمليا دون تغيير من عام 1997 إلى عام 1999. وفي نفس الوقت ، انخفضت النسبة المئوية لدخول المستشفى للمرضى الذين يعانون من احتشاء عضلة القلب غير المصحوب بمضاعفات بنسبة 6.6٪ من عام 1997 إلى عام 1999.
الجدول 1. هيكل المكالمات لمرضى MI.
|
فِهرِس |
1997 |
1998 |
1999 |
|
عدد المكالمات لمرضى MI |
|||
|
غير معقد |
16255 |
16156 |
16172 |
|
معقد |
7375 |
7383 |
7318 |
|
المجموع |
23630 |
23539 |
23490 |
|
٪ من إجمالي عدد مرضى القلب والأوعية الدموية |
|||
|
المرضى في المستشفى |
|||
|
MI غير معقد |
11853 |
12728 |
11855 |
|
معقد MI |
3516 |
1593 |
3623 |
|
المجموع |
15369 |
16321 |
15478 |
|
النسبة المئوية للمرضى المقيمين في المستشفى إلى عدد المكالمات |
|||
|
MI غير معقد |
79,9 |
78,8 |
73,3 |
|
معقد MI |
47,6 |
48,7 |
49,5 |
|
المجموع |
65,0 |
69,3 |
65,9 |
تعريف
احتشاء عضلة القلب هو حالة سريرية ملحة ناتجة عن نخر جزء من عضلة القلب نتيجة لانتهاك إمدادات الدم.
الأسباب الرئيسية ومسببات الأمراض
التطور كجزء من أمراض القلب التاجية ، هو نتيجة لمرض القلب التاجي. غالبًا ما يكون السبب المباشر لاحتشاء عضلة القلب هو انسداد الشريان التاجي أو تضيقه الفرعي ، والذي يحدث دائمًا تقريبًا بسبب التمزق أو الانقسام. لوحة تصلب الشرايينمع تكوين خثرة ، وزيادة تراكم الصفائح الدموية وتشنج قطعي بالقرب من البلاك.
تصنيف
من وجهة نظر تحديد مقدار العلاج الدوائي الضروري وتقييم الإنذار ، هناك ثلاثة تصنيفات ذات أهمية.
A. من عمق الآفة (بناءً على بيانات تخطيط القلب):
1. عبر النقل والبؤرة الكلية ("Q-infarction") - مع ظهور المقطع ST في
الساعات الأولى للمرض وتشكيل موجة Q في المستقبل.
2. بؤري صغير ("ليس احتشاء Q") - غير مصحوب بتكوين موجة Q ، ولكن
يتجلى من خلال موجات T السلبية
حسب المقرر السريري:
1. احتشاء عضلة القلب غير المصحوب بمضاعفات.
2. احتشاء عضلة القلب المعقد (انظر أدناه).
ب. بالتوطين:
1. احتشاء البطين الأيسر (أمامي ، خلفي أو سفلي ، حاجز)
2. احتشاء البطين الأيمن.
الصورة السريرية
وفقًا لأعراض المرحلة الأكثر حدة من احتشاء عضلة القلب ، يتم تمييز المتغيرات السريرية التالية:
|
ألم (حالة anginosus) |
- مسار سريري نموذجي ، وأهم مظاهره هو ألم الزاوي ، بغض النظر عن الوضعية و وضع الجسم، ضد الحركة والتنفس ، مقاومة للنترات. الألم له طابع ضاغط أو خانق أو حارق أو تمزق مع توطين خلف القص ، في جدار الصدر الأمامي بالكامل مع إمكانية تشعيع الكتفين والرقبة والذراعين والظهر والمنطقة الشرسوفية ؛ يتميز بمزيج من فرط التعرق ، والضعف العام الشديد ، وشحوب الجلد ، والإثارة ، والأرق الحركي. |
|
البطن (حالة المعدة) |
- يتجلى من خلال مزيج من الألم الشرسوفي مع أعراض عسر الهضم - الغثيان والقيء الذي لا يجلب الراحة والفواق والتجشؤ والانتفاخ الشديد ؛ تشعيع ممكن من آلام الظهر والتوتر جدار البطنوألم عند الجس في المنطقة الشرسوفية ذلك الجزء فوق المعدة. |
|
ألم غير نمطي |
- حيث تكون متلازمة الألم ذات طابع غير نمطي من حيث التوطين (على سبيل المثال ، فقط في مناطق التشعيع - الحلق والفك السفلي والكتفين والذراعين وما إلى ذلك) و / أو في الطبيعة. |
|
الربو (حالة ربوية) |
- العلامة الوحيدة التي فيها نوبة ضيق في التنفس ، والتي هي مظهر من مظاهر قصور القلب الاحتقاني الحاد (الربو القلبي أو الوذمة الرئوية). |
|
عدم انتظام ضربات القلب |
- حيث تكون اضطرابات الإيقاع هي الوحيدة مظاهر سريريةأو تهيمن على الصورة السريرية. |
|
الأوعية الدموية الدماغية |
- الصورة السريرية التي تهيمن عليها علامات الحوادث الوعائية الدماغية (غالبًا ما تكون ديناميكية): الإغماء ، والدوخة ، والغثيان ، والقيء ؛ الأعراض العصبية البؤرية المحتملة. |
|
بدون أعراض (بدون أعراض) |
- المتغير الأكثر صعوبة في التعرف عليه ، وغالبًا ما يتم تشخيصه بأثر رجعي وفقًا لبيانات تخطيط القلب. |
معايير التشخيص
في مرحلة الرعاية الطبية قبل دخول المستشفى ، يتم تشخيص احتشاء عضلة القلب الحاد على أساس وجود:
أ) الصورة السريرية
ب) التغييرات في مخطط القلب الكهربائي.
أ. المعايير السريرية.
مع ألم متغير من احتشاء عضلة القلب د لها قيمة تشخيصية:
- شدة (في الحالات التي حدثت فيها آلام مماثلة في وقت سابق ، مع نوبة قلبية تكون شديدة بشكل غير عادي) ،
- المدة (بشكل غير عادي هجوم مطولتدوم أكثر من 15-20 دقيقة) ،
- سلوك المريض (الإثارة ، الأرق) ،
- فشل تناول النترات تحت اللسان.
الجدول 2.
قائمة الأسئلة المطلوبة في تحليل الألم في حالة الاشتباه باحتشاء عضلة القلب الحاد
|
سؤال |
ملحوظة |
|
متى بدأت النوبة؟ |
من المستحسن أن تحدد بدقة قدر الإمكان. |
|
كم من الوقت يستمر الهجوم؟ |
أقل من 15 أو 15-20 أو أكثر من 20 دقيقة. |
|
هل كانت هناك محاولات لوقف هجوم النتروجليسرين؟ |
هل كان هناك تأثير قصير المدى؟ |
|
هل يعتمد الألم على الموقف ، ووضعية الجسم ، والحركة ، والتنفس؟ |
لا تعتمد على هجوم التاجي. |
|
هل حدثت نوبات مماثلة في الماضي؟ |
تتطلب هجمات مماثلة لا تنتهي بنوبة قلبية تشخيص متباينمع الذبحة الصدرية غير المستقرة وأسباب غير قلبية. |
|
هل حدثت نوبات (ألم أو اختناق) أثناء النشاط البدني(المشي) ، هل أجبروهم على التوقف ، إلى متى استمروا (بالدقائق) ، كيف تفاعلوا مع النتروجليسرين؟ |
يؤدي وجود الذبحة الصدرية الجهدية إلى احتمال حدوث احتشاء عضلة القلب الحاد. |
|
هل الهجوم الحقيقي يشبه الأحاسيس التي نشأت أثناء المجهود البدني من حيث توطين أو طبيعة الألم؟ |
من حيث الشدة والأعراض المصاحبة ، عادة ما تكون النوبة في احتشاء عضلة القلب أكثر حدة منها في الذبحة الصدرية. |
لأي خيار مساعد قيمة التشخيصيملك:
فرط التعرق ،
ضعف عام شديد
شحوب الجلد
علامات قصور القلب الحاد.
لا يمكن أن يكون عدم وجود صورة سريرية نموذجية بمثابة دليل على عدم وجود احتشاء عضلة القلب.
معايير تخطيط القلب الكهربائي - التغييرات التي تكون بمثابة علامات:
|
ضرر |
- الارتفاع المقوس للجزء ST مع انتفاخ للأعلى ، أو الاندماج مع موجة T موجبة أو التحول إلى موجة T سالبة (من الممكن حدوث انخفاض مقوس للجزء ST مع انتفاخ لأسفل) ؛ |
|
ماكروفوكال أو احتشاء بطاني |
- ظهور موجة مرضية Q وانخفاض في اتساع الموجة R أو اختفاء الموجة R وتشكيل QS ؛ |
|
احتشاء بؤري صغير |
- ظهور موجة T متناظرة سلبية ؛ |
|
ملحوظات: 1. علامة غير مباشرة على احتشاء عضلة القلب ، والتي لا تسمح بتحديد مرحلة وعمق العملية ، هي حصار حاد لأرجل حزمته (في وجود عيادة مناسبة). 2. تتمتع بيانات تخطيط القلب في الديناميكيات بأكبر قدر من الموثوقية ، لذلك يجب مقارنة مخطط كهربية القلب مع البيانات السابقة كلما أمكن ذلك. |
|
مع احتشاء الجدار الأمامي ، يتم الكشف عن هذه التغييرات في الخيوط القياسية I و II ، والرصاص المعزز من اليد اليسرى (aVL) وأسلاك الصدر المقابلة (V1 ، 2 ، 3 ، 4 ، 5 ، 6). في حالة احتشاء عضلة القلب الجانبي المرتفع ، لا يمكن تسجيل التغييرات إلا في مسار ضغط القلب الأيسر ، ويجب إزالة خيوط الصدر المرتفعة لتأكيد التشخيص. مع احتشاء الجدار الخلفي (السفلي ، الحجاب الحاجز) ، تم العثور على هذه التغييرات في معيار II و III وخيوط محسّنة من القدم اليمنى(aVF). في حالة احتشاء عضلة القلب للأقسام العالية من الجدار الخلفي للبطين الأيسر (الخلفي - القاعدية) ، لا يتم تسجيل أي تغييرات في الخيوط القياسية ، ويتم التشخيص على أساس التغييرات المتبادلة - موجات R و T عالية في الخيوط V 1 - الخامس 2 (الجدول 3).
أرز. 1. المرحلة الأكثر حدة من احتشاء عضلة القلب الأمامي عبر الجافية.
الجدول 3. توطين احتشاء عضلة القلب وفقا لبيانات تخطيط القلب
|
نوع الاحتشاء حسب التوطين |
يؤدي القياسية |
يؤدي الصدر |
|||||||||
|
ثالثا |
|||||||||||
|
الحاجز |
|||||||||||
|
بيردن الحاجز |
|||||||||||
|
أمام |
|||||||||||
|
الأمامي المشترك |
|||||||||||
|
الأمامي والجانبي |
|||||||||||
|
جانب |
|||||||||||
|
جانب مرتفع |
|||||||||||
|
الخلفي الجانبي |
|||||||||||
|
الحجاب الحاجز الخلفي |
|||||||||||
|
الخلفي القاعدية |
|||||||||||
علاج احتشاء عضلة القلب
العلاج في حالات الطوارئ له عدة أهداف مترابطة:
1. الحجامة متلازمة الألم.
2. استعادة تدفق الدم في الشريان التاجي.
3. انخفاض في عمل القلب والطلب على الأوكسجين لعضلة القلب.
4. الحد من حجم احتشاء عضلة القلب.
5. العلاج والوقاية من مضاعفات احتشاء عضلة القلب.
يتم عرض الأدوية المستخدمة لهذا في الجدول 3.
الجدول 3
الاتجاهات الرئيسية للعلاج والأدوية المستخدمة في المرحلة الحادة من احتشاء عضلة القلب غير المصحوب بمضاعفات
|
الدواء |
اتجاهات العلاج |
|
|
المورفين عن طريق الوريد كسور |
تخفيف الآلام بشكل كافٍ ، وتقليل الحمل قبل وبعد الحمل ، والانفعالات الحركية النفسية ، والطلب على الأكسجين لعضلة القلب |
2-5 مجم في الوريد كل 5-15 دقيقة حتى تختفي متلازمة الألم تمامًا أو حتى آثار جانبية |
|
الستربتوكيناز (الستربتاز) |
استعادة تدفق الدم التاجي (تجلط الدم) ، وتخفيف الآلام ، والحد من حجم احتشاء عضلة القلب ، وتقليل الوفيات |
1.5 مليون وحدة دولية خلال 60 دقيقة |
|
بلعة الهيبارين في الوريد (إذا لم يتم إجراء تحلل الخثرة) |
منع أو الحد من تجلط الدم التاجي ، والوقاية من مضاعفات الانصمام الخثاري ، وتقليل الوفيات |
10000-15000 وحدة دولية عن طريق الوريد عن طريق التيار |
|
نيتروجليسرين أو إيزوسوربيد ثنائي النترات عن طريق الوريد |
تخفيف الآلام وتقليل حجم احتشاء عضلة القلب والوفيات |
10 ميكروغرام / دقيقة. مع زيادة السرعة بمقدار 20 ميكروجرام / دقيقة كل 5 دقائق تحت سيطرة معدل ضربات القلب وضغط الدم |
|
حاصرات بيتا: بروبرانولول (Obzidan) |
انخفاض الطلب على الأكسجين في عضلة القلب ، وتخفيف متلازمة الألم ، وتقليل حجم النخر ، والوقاية من الرجفان البطيني وتمزق البطين الأيسر ، واحتشاء عضلة القلب المتكرر ، وانخفاض معدل الوفيات |
1 مجم / دقيقة كل 3 إلى 5 دقائق حتى جرعة إجمالية قدرها 10 مجم |
|
حمض أسيتيل الساليسيليك (الأسبرين) |
الإغاثة والوقاية من العمليات المرتبطة بتكدس الصفائح الدموية ؛ مع موعد مبكر (!) يقلل الوفيات |
160-325 مجم مضغ ؛ |
|
المغنيسيوم كبريتات (كورماغنيزين) |
انخفاض الطلب على الأكسجين في عضلة القلب ، وتخفيف الآلام ، وتقليل النخر ، والوقاية من الاضطرابات معدل ضربات القلب، قصور القلب ، انخفاض معدل الوفيات |
1000 مجم مغنيسيوم (50 مل 10٪ ، 25 مل 20٪ أو 20 مل محلول 25٪) عن طريق الوريد لمدة 30 دقيقة. |
ALGORITHM لتقديم الرعاية الطبية للمرضى الذين يعانون من احتشاء عضلة القلب الحاد في مرحلة ما قبل المستشفى
أ- احتشاء عضلة القلب غير المعقد
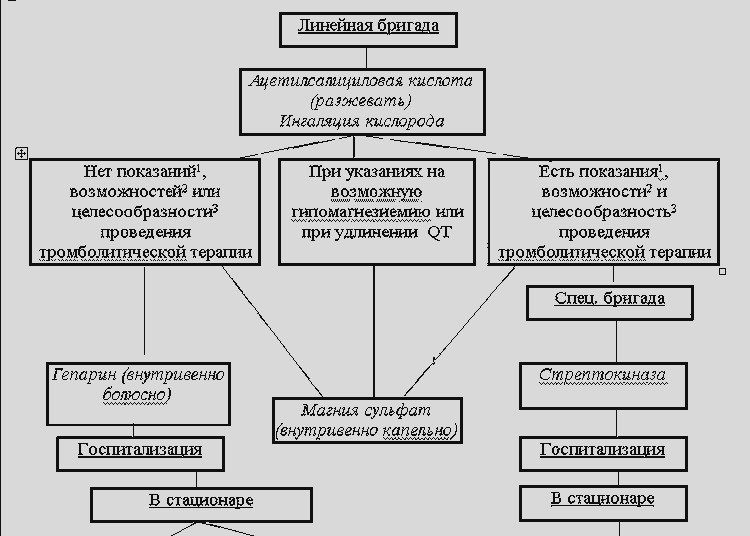

ب. احتشاء عضلة القلب غير معقد أواحتشاء عضلة القلب معقد بسبب متلازمة الألم المستمر

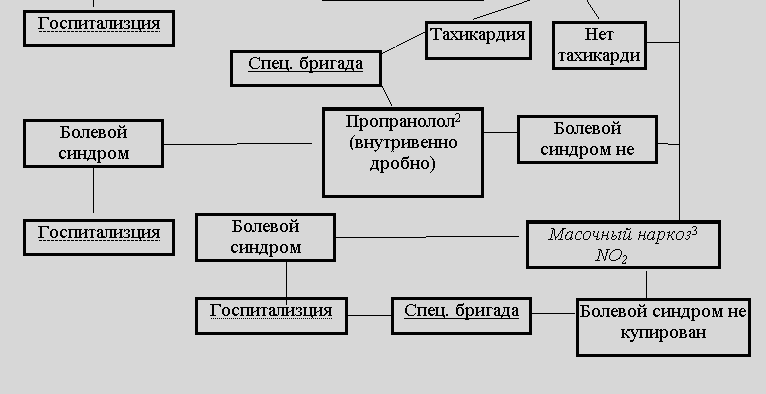
ب. احتشاء عضلة القلب المعقد

1. تخفيف نوبة الألم
في احتشاء عضلة القلب الحاد - واحدة من أهم المهام ، حيث أن الألم من خلال تنشيط الجهاز الودي الوعائي يؤدي إلى زيادة مقاومة الأوعية الدموية وتكرار وقوة تقلصات القلب ، أي أنه يزيد من الحمل الديناميكي الدموي على القلب ، ويزيد من أكسجين عضلة القلب الطلب وتفاقم نقص التروية.
إذا لم يؤد تناول النتروجليسرين الأولي تحت اللسان (مرارًا وتكرارًا عند 0.5 مجم في الأقراص أو 0.4 مجم في الهباء الجوي) إلى إيقاف الألم ، يبدأ العلاج بالمسكنات المخدرة ، والتي ، بالإضافة إلى التأثيرات المسكنة والمهدئة ، لها تأثير على ديناميكا الدم: بسبب توسع الأوعية الخصائص ، فهي توفر تفريغ الدورة الدموية لعضلة القلب ، مما يقلل من التحميل المسبق في المقام الأول. في مرحلة ما قبل دخول المستشفى ، يكون الدواء المفضل لتخفيف الألم في احتشاء عضلة القلب هو المورفين ، والذي ليس له التأثيرات الضرورية فحسب ، بل له أيضًا مدة عمل كافية للنقل. يتم إعطاء الدواء عن طريق الوريد كسور: يتم تخفيف 1 مل من محلول 1 ٪ بمحلول كلوريد الصوديوم الفسيولوجي إلى 20 مل (يحتوي 1 مل من المحلول الناتج على 0.5 مجم من المادة الفعالة) ويتم إعطاء 2-5 مجم كل 5-15 مجم دقائق حتى يتم القضاء على متلازمة الألم تمامًا أو حتى ظهور أعراض جانبية (انخفاض ضغط الدم ، تثبيط تنفسي ، قيء). يجب ألا تتجاوز الجرعة الإجمالية 10-15 مجم (1-1.5 مل من محلول 1٪) من المورفين (في مرحلة ما قبل المستشفى ، يجب عدم تجاوز جرعة 20 مجم).
مع متلازمة الألم غير المعلنة ، ومرضى الشيخوخة والمرضى المنهكين ، يمكن إعطاء المسكنات المخدرة تحت الجلد أو في العضل. لا ينصح بحقن أكثر من 60 ملغ من المورفين تحت الجلد خلال 12 ساعة.
للوقاية والتخفيف من الآثار الجانبية للمسكنات المخدرة مثل الغثيان والقيء ، يوصى بإعطاء 10-20 ملغ من ميتوكلوبراميد (، راجلان) في الوريد. في بطء القلب الشديدمع أو بدون انخفاض ضغط الدم ، يشار إلى استخدام الأتروبين بجرعة 0.5 مجم (0.5 مل من محلول 0.1 ٪) عن طريق الوريد ؛ تتم مكافحة انخفاض ضغط الدم وفقًا للمبادئ العامة لتصحيح انخفاض ضغط الدم في حالة احتشاء عضلة القلب.
الفعالية غير الكافية للتخدير بالمسكنات المخدرة هي مؤشر على التسريب الوريدي للنترات. مع انخفاض كفاءة النترات مع عدم انتظام دقات القلب ، يمكن الحصول على تأثير مسكن إضافي عن طريق إدخال حاصرات بيتا. يمكن تخفيف الألم عن طريق تحلل الخثرة الفعال.
مكثفة مستمرة ألم في الذبحة الصدريةيعمل كمؤشر لاستخدام قناع التخدير بأكسيد النيتروز (الذي له تأثير مهدئ ومسكن) ممزوج بالأكسجين. ابدأ باستنشاق الأكسجين لمدة 1-3 دقائق ، ثم استخدم أكسيد النيتروز (20٪) مع الأكسجين (80٪) مع زيادة تدريجية في تركيز أكسيد النيتروز إلى 80٪ ؛ بعد أن ينام المريض ، يتحول إلى تركيز غازات صيانة - 50´ 50٪. على الجانب الإيجابي ، لا يؤثر أكسيد النيتروز على وظيفة البطين الأيسر. حدوث آثار جانبية - غثيان ، قيء ، هياج أو ارتباك - هو مؤشر على تقليل تركيز أكسيد النيتروز أو وقف الاستنشاق. عند ترك التخدير ، يتم استنشاق الأكسجين النقي لمدة 10 دقائق لمنع نقص تأكسج الدم الشرياني.
لحل مسألة إمكانية استخدام المسكنات المخدرة ، يجب توضيح عدد من النقاط:
- تأكد من أن متلازمة الألم النموذجية أو غير النمطية ليست مظهرًا من مظاهر "البطن الحاد" ، وأن تغييرات تخطيط القلب هي مظهر محدد لاحتشاء عضلة القلب ، وليست رد فعل غير محدد لكارثة في تجويف البطن ؛
- اكتشف ما إذا كان هناك تاريخ الأمراض المزمنةالجهاز التنفسي ، على وجه الخصوص ، الربو القصبي.
- توضيح متى كان آخر تفاقم لمتلازمة انسداد القصبات الهوائية ؛
- لتحديد ما إذا كانت هناك حاليًا علامات على فشل الجهاز التنفسي ، وما هي درجة شدتها ؛
- معرفة ما إذا كان المريض لديه تاريخ من متلازمة التشنج ، متى كانت النوبة الأخيرة.
2. استعادة تدفق الدم التاجي في المرحلة الحادة من احتشاء عضلة القلب ،
يتم إجراء تحسين كبير في التشخيص ، في حالة عدم وجود موانع ، عن طريق تخثر الدم النظامي.
أ). مؤشرات تحلل الخثرة هي وجود ارتفاع للجزء ST يزيد عن 1 مم في اثنين على الأقل من موصلي مخطط كهربية القلب القياسيين وأكثر من 2 مم في اثنين من خيوط الصدر المجاورة أو انسداد كامل حاد لكتلة فرع الحزمة اليسرى في الفترة التي انقضت منذ ظهور المرض أكثر من 30 دقيقة ولكن ليس أكثر من 12 ساعة. يمكن استخدام عوامل الحالة للتخثر لاحقًا في الحالات التي يستمر فيها ارتفاع المقطع ST ، واستمرار الألم و / أو ملاحظة ديناميكا الدم غير المستقرة.
على عكس تحلل الخثرة الجهازي داخل التاج (الذي يتم إجراؤه عن طريق الحقن الوريدي لعوامل الحالة للتخثر) لا يتطلب أي تلاعبات معقدة ومعدات خاصة. في الوقت نفسه ، يكون فعالًا تمامًا إذا بدأ في الساعات الأولى من تطور احتشاء عضلة القلب (على النحو الأمثل - في مرحلة ما قبل المستشفى) ، نظرًا لأن انخفاض معدل الوفيات يعتمد بشكل مباشر على توقيت ظهوره.
في حالة عدم وجود موانع ، يعتمد قرار إجراء تحلل الخثرة على تحليل عامل الوقت: إذا كان النقل إلى المستشفى المناسب قد يكون أطول من الفترة التي سبقت بدء هذا العلاج من قبل فريق إسعاف متخصص (مع وقت نقل تقديري) لأكثر من 30 دقيقة أو إذا تأخر تحلل الخثرة في المستشفى لأكثر من 60 دقيقة) ، يجب أن يتم إدخال العوامل الحالة للتخثر في مرحلة الرعاية الطبية قبل دخول المستشفى. وإلا يجب تأجيلها حتى مرحلة المستشفى.
الستربتوكيناز هو الأكثر استخدامًا. طريقة إعطاء الستربتوكيناز عن طريق الوريد: يتم إدخال الستربتوكيناز فقط من خلال الأوردة المحيطية ، ومحاولات قسطرة الأوردة المركزية غير مقبولة ؛ قبل التسريب ، يمكن إعطاء 5-6 مل من 25 ٪ كبريتات المغنيسيوم في الوريد ، أو 10 مل من cormagnesin-200 عن طريق الوريد ، ببطء (لمدة 5 دقائق) ؛ تعطى دائما جرعة "تحميل" من الأسبرين (250-300 ملغ - مضغ) ، إلا في حالة بطلان الأسبرين (للحساسية و) ؛ يتم تخفيف 1500000 وحدة من الستربتوكيناز في 100 مل من محلول كلوريد الصوديوم متساوي التوتر ويتم إعطاؤها عن طريق الوريد لمدة 30 دقيقة.
التعيين المتزامن للهيبارين عند استخدام الستربتوكيناز غير مطلوب - من المفترض أن الستربتوكيناز نفسه له خصائص مضادة للتخثر ومضادة للتجمّع. لقد ثبت أن إعطاء الهيبارين عن طريق الوريد لا يقلل من معدل الوفيات وتكرار احتشاء عضلة القلب ، وفعالية إعطائه تحت الجلد مشكوك فيها. إذا تم إدخال الهيبارين في وقت سابق لسبب ما ، فهذا لا يمثل عقبة أمام تحلل الخثرة. من المستحسن أن يتم وصف الهيبارين بعد 4 ساعات من نهاية ضخ الستربتوكيناز. تم التعرف على استخدام الهيدروكورتيزون الموصى به سابقًا للوقاية من الحساسية المفرطة ليس فقط على أنه غير فعال ، ولكنه أيضًا غير آمن في المرحلة الحادة من احتشاء عضلة القلب (تزيد الجلوكوكورتيكويد من خطر تمزق عضلة القلب).
المضاعفات الرئيسية لانحلال الخثرة
1). النزيف (بما في ذلك الأكثر رعبا - داخل الجمجمة) - يتطور نتيجة لتثبيط عمليات تخثر الدم وانحلال الجلطات الدموية. يبلغ خطر الإصابة بسكتة دماغية مع تحلل الخثرة الجهازي 0.5-1.5٪ من الحالات ، وعادة ما تحدث السكتة الدماغية في اليوم الأول بعد تحلل الخثرة. لوقف النزيف البسيط (من موقع البزل ، من الفم والأنف) ، يكفي ضغط منطقة النزيف. مع نزيف أكثر خطورة (معدي معوي ، داخل الجمجمة) ، يكون التسريب الوريدي لحمض أمينوكابرويك ضروريًا - يتم إعطاء 100 مل من محلول 5 ٪ خلال 30 دقيقة ثم 1 جم / ساعة حتى يتوقف النزيف ، أو حمض الترانيكساميك 1-1.5 جم 3-4 مرة واحدة في اليوم بالتنقيط عن طريق الوريد. بالإضافة إلى ذلك ، فإن نقل البلازما الطازجة المجمدة فعال. ومع ذلك ، يجب أن نتذكر أنه عند استخدام عوامل مضادات انحلال الفبرين ، يزداد خطر إعادة انسداد الشريان التاجي وإعادة احتشاءه ، لذلك يجب استخدامها فقط مع نزيف يهدد الحياة.
2). عدم انتظام ضربات القلب الذي يحدث بعد استعادة الدورة الدموية التاجية (ضخه). لا تتطلب العناية المركزة إيقاعًا بطيئًا من العقدة أو البطين (مع معدل ضربات القلب أقل من 120 في الدقيقة وديناميكا الدم المستقرة) ؛ انقباض خارج البطين فوق البطيني (بما في ذلك اللانظمي) ؛ الإحصار الأذيني البطيني الأول والثاني (نوع موبيتز الأول) درجة. يتطلب الرعاية في حالات الطوارئالرجفان البطيني (يتطلب إزالة الرجفان ، مجموعة من إجراءات الإنعاش القياسية) ؛ تسرع القلب البطيني المغزلي ثنائي الاتجاه من النوع "الدوران" (يظهر إزالة الرجفان ، إدخال بلعة في الوريد من كبريتات المغنيسيوم) ؛ أصناف أخرى عدم انتظام دقات القلب البطيني(استخدم إدخال الليدوكائين أو قم بإجراء تقويم نظم القلب) ؛ تسرع القلب فوق البطيني المستمر (توقف عن طريق الحقن الوريدي للفيراباميل أو نوفوكيناميد) ؛ الحصار الأذيني البطيني الثاني (موبيتز من النوع الثاني) والدرجة الثالثة ، الحصار الجيبي الأذيني (يتم حقن الأتروبين عن طريق الوريد بجرعة تصل إلى 2.5 مجم ، إذا لزم الأمر ، يتم إجراء سرعة طارئة).
3). ردود الفعل التحسسية. طفح جلدي ، حكة ، وذمة حول الحجاج تحدث في 4.4٪ من الحالات ، ردود فعل شديدة (، صدمة الحساسية) - في 1.7٪ من الحالات. في حالة الاشتباه في حدوث تفاعل تأقاني ، يجب إيقاف تسريب الستربتوكيناز على الفور وإعطاء جرعة من 150 ملغ من بريدنيزولون عن طريق الوريد. في حالة تثبيط الدورة الدموية الحاد وظهور علامات الصدمة التأقية ، يتم إعطاء 1 مل من محلول 1 ٪ من الأدرينالين عن طريق الوريد ، مع استمرار الإعطاء هرمونات الستيرويدتقطير وريدي. يتم علاج الحمى بالأسبرين أو الباراسيتامول.
4). يتم إيقاف تكرار الألم بعد تجلط الدم عن طريق الحقن الوريدي الجزئي للمسكنات المخدرة. مع زيادة التغيرات الإقفارية على مخطط كهربية القلب ، يشار إلى إعطاء النتروجليسرين بالتنقيط في الوريد أو ، إذا كان التسريب مثبتًا بالفعل ، يتم زيادة معدل إدارته.
5). مع انخفاض ضغط الدم الشرياني ، يكفي في معظم الحالات إيقاف التسريب الحالة للخثرة ورفع ساقي المريض ؛ إذا لزم الأمر ، يتم تصحيح مستوى ضغط الدم عن طريق إدخال السوائل أو عوامل ضغط الأوعية (الدوبامين أو النوربينفرين عن طريق الوريد بالتنقيط حتى يستقر ضغط الدم الانقباضي عند 90-100 مم زئبق).

أرز. 2. عدم انتظام ضربات ضخ الدم في احتشاء عضلة القلب الخلفي عبر الجيوب: حلقة من الإيقاع الوصلي مع استعادة مستقلة لإيقاع الجيوب الأنفية.
العلامات السريرية لاستعادة تدفق الدم التاجي:
- وقف النوبات الخلقية بعد 30-60 دقيقة من تناول الحالة التخثرية ،
- استقرار ديناميكا الدم ،
- اختفاء علامات فشل البطين الأيسر ،
- سريع (خلال عدة ساعات) ديناميات تخطيط القلب مع اقتراب مقطع ST من العزلة وتشكيل موجة Q المرضية ، الشق السلبي T (ربما زيادة مفاجئة في درجة ارتفاع المقطع ST ، متبوعًا بانخفاضها السريع) ،
- ظهور عدم انتظام ضربات القلب (إيقاع بطني متسارع ، انقباض البطين ، إلخ) ،
- الديناميكيات السريعة لـ CF-CPK (زيادة حادة في نشاطها بنسبة 20-40 ٪).
لحل مشكلة إمكانية استخدام عوامل التخثر ، يجب توضيح عدد من النقاط:
- تأكد من عدم وجود نزيف داخلي حاد خلال الأيام العشرة السابقة - الجهاز الهضمي والرئوي والرحمي ، باستثناء الدورة الشهرية والبيلة الدموية وما إلى ذلك (انتبه إلى تاريخهم) أو التدخلات الجراحية والإصابات التي تلحق الضرر بالأعضاء الداخلية ؛
- استبعاد التواجد خلال الشهرين الماضيين من الحوادث الوعائية الدماغية الحادة أو الجراحة أو الصدمة للدماغ أو النخاع الشوكي (انتبه لتاريخهم) ؛
- استبعاد الاشتباه في التهاب البنكرياس الحاد وتشريح تمدد الأوعية الدموية الأبهري وكذلك تمدد الأوعية الدموية في الشريان الدماغي أو أورام المخ أو الأورام الخبيثة المنتشرة ؛
- إثبات عدم وجود علامات جسدية أو مؤشرات مرضية لأمراض نظام تخثر الدم - أهبة نزفية ، قلة الصفيحات (انتبه إلى اعتلال الشبكية السكري النزفي) ؛
- تأكد من أن المريض لا يتلقى مضادات التخثر غير المباشرة ؛
- لتوضيح ما إذا كانت هناك أي ردود فعل تحسسية تجاه الأدوية الحالة للخثرة المقابلة ، وفيما يتعلق بالستربتوكيناز ، ما إذا كانت هناك إدارة سابقة من 5 أيام إلى سنتين (خلال هذه الفترة ، نظرًا لارتفاع عيار الأجسام المضادة ، فإن إعطاء الستربتوكيناز هو غير مقبول)؛
- في حالة إجراءات الإنعاش الناجحة ، تأكد من أنها لم تكن مؤلمة وطويلة الأمد (في حالة عدم وجود علامات إصابات ما بعد الإنعاش - كسور في الأضلاع وتلف في الأعضاء الداخلية ، انتبه لمدة تزيد عن 10 دقائق) ؛
- تحقيق استقرار ضغط الدم المرتفع عند مستوى أقل من 200/120 ملم زئبق. فن. (انتبه للمستوى الذي يتجاوز 180/110 ملم زئبق فن.)
- انتبه للحالات الأخرى التي تشكل خطورة على تطور المضاعفات النزفية وتكون بمثابة موانع نسبية لتخثر الدم الجهازي: أمراض خطيرةالكبد أو الكلى. اشتباه في تمدد الأوعية الدموية المزمن في القلب ، والتهاب التامور ، والتهاب عضلة القلب المعدية ، ووجود جلطة في تجاويف القلب. التهاب الوريد الخثاري والتخثر الوريدي. دوالي المريء ، قرحة هضمية في المرحلة الحادة. حمل؛
- ضع في اعتبارك أن عددًا من العوامل التي ليست موانع نسبية أو مطلقة لانحلال الخثرة الجهازي قد تزيد من مخاطره: العمر فوق 65 عامًا ، ووزن الجسم أقل من 70 كجم ، والجنس الأنثوي ، وارتفاع ضغط الدم الشرياني.
يمكن حدوث تجلط الدم الجهازي في كبار السن والشيخوخة ، وكذلك على خلفية انخفاض ضغط الدم الشرياني (ضغط الدم الانقباضي أقل من 100 ملم زئبق) والصدمة القلبية.
في الحالات المشكوك فيها ، يجب تأجيل قرار إجراء العلاج حال التخثر حتى مرحلة العلاج للمرضى الداخليين. يشار إلى التأخير لتطور المرض غير النمطي ، والتغيرات غير المحددة في مخطط كهربية القلب ، وإحصار الحزم طويل الأمد ، واحتشاء عضلة القلب السابق الواضح الذي يخفي التغييرات النموذجية.
ب). عدم وجود مؤشرات للعلاج حال التخثر (المصطلحات المتأخرة ، ما يسمى بؤري صغير أو احتشاء غير Q) ، واستحالة تجلط الدم لأسباب تنظيمية ، وكذلك تأخره حتى مرحلة المستشفى أو بعض موانع استخدامه ، والتي ليست موانع لتعيين الهيبارين ، تعمل كمؤشر (في حالة عدم وجود موانع خاصة) للعلاج المضاد للتخثر. والغرض منه هو منع أو الحد من تجلط الشرايين التاجية ، وكذلك منع مضاعفات الانسداد التجلطي (خاصة في المرضى الذين يعانون من احتشاء عضلة القلب الأمامي ، مع انخفاض النتاج القلبي ، والرجفان الأذيني). للقيام بذلك ، في مرحلة ما قبل دخول المستشفى (الفريق الخطي) ، يتم إعطاء الهيبارين عن طريق الوريد كبلعة بجرعة 10000-15000 وحدة دولية. إذا لم يتم تنفيذ العلاج الحالة للخثرة في المستشفى ، فإنهم يتحولون إلى الحقن الوريدي طويل الأمد للهيبارين بمعدل 1000 وحدة دولية / ساعة تحت سيطرة زمن الثرومبوبلاستين الجزئي المنشط. قد يكون البديل ، على ما يبدو ، هو إعطاء الهيبارين منخفض الوزن الجزيئي تحت الجلد في جرعة "علاجية". لا يمثل إدخال الهيبارين في مرحلة ما قبل دخول المستشفى عقبة أمام انحلال الخثرة في المستشفى.
على الرغم من السلامة العالية للعلاج بالهيبارين مقارنةً بانحلال الخثرة الجهازي ، نظرًا لفعاليته الأقل بشكل ملحوظ ، فإن عددًا من موانع استخدامه أكثر صرامة ، وبعض الموانع النسبية لتحلل الخثرة تبين أنها مطلقة لعلاج الهيبارين. من ناحية أخرى ، يمكن وصف الهيبارين للمرضى الذين يعانون من بعض موانع استخدام عوامل التخثر.
لحل مشكلة إمكانية وصف الهيبارين ، يجب توضيح نفس النقاط بالنسبة للعوامل الحالة للتخثر:
- استبعاد تاريخ السكتة الدماغية النزفية ، وعمليات الدماغ والحبل الشوكي ؛
- تأكد من عدم وجود ورم وقرحة هضمية في المعدة والاثني عشر ، والتهاب الشغاف المعدي ، والتلف الشديد للكبد والكلى ؛
- استبعاد الاشتباه في التهاب البنكرياس الحاد ، تشريح تمدد الأوعية الدموية الأبهري ، التهاب التامور الحاد مع سماع احتكاك التامور لعدة أيام (!) (خطر الإصابة بتطور دموية القلب) ؛
- إثبات عدم وجود علامات جسدية أو مؤشرات عابرة لأمراض نظام تخثر الدم (أهبة النزفية وأمراض الدم) ؛
معرفة ما إذا كان المريض يعاني من فرط الحساسية للهيبارين ؛
- تحقيق استقرار ضغط الدم المرتفع عند مستوى أقل من 200/120 ملم زئبق. فن.
في). من الدقائق الأولى لاحتشاء عضلة القلب ، يُظهر لجميع المرضى في حالة عدم وجود موانع استخدام جرعات صغيرة من حمض أسيتيل الساليسيليك (الأسبرين) ، والذي يصل تأثيره المضاد للصفيحات إلى الحد الأقصى بعد 30 دقيقة ويمكن أن يؤدي البدء في الوقت المناسب إلى تقليل الوفيات بشكل كبير . يمكن الحصول على أكبر تأثير سريري باستخدام حمض أسيتيل الساليسيليك قبل تحلل الخثرة. جرعة الجرعة الأولى في مرحلة ما قبل دخول المستشفى هي 160-325 مجم ، مضغ (!). في وقت لاحق ، في المرحلة الثابتة ، يوصف الدواء مرة واحدة يوميًا مقابل 100-125 مجم.
لحل مشكلة إمكانية وصف حمض أسيتيل الساليسيليك ، لا يهم سوى جزء صغير من القيود المفروضة على العوامل الحالة للتخثر ؛ يحتاج إلى توضيح:
هل يعاني المريض من آفات تآكلي وتقرحي في الجهاز الهضمي في المرحلة الحادة؟
ما إذا كان هناك تاريخ من نزيف الجهاز الهضمي.
هل يعاني المريض من فقر الدم؟
- هل يعاني المريض من "ثالوث الأسبرين" (، داء السلائل الأنفي ،
عدم تحمل الأسبرين) ؛
هل هناك حساسية تجاه الدواء؟
3. انخفاض معدل ضربات القلب والطلب على الأوكسجين لعضلة القلب
بالإضافة إلى التخدير الكامل يتم توفيره عن طريق استخدام
أ) موسعات الأوعية - النترات ،
ب) حاصرات بيتا و
ج) وسائل العمل المعقد - كبريتات المغنيسيوم.
A. الحقن في الوريد من النتراتفي حالة احتشاء عضلة القلب الحاد ، فهو لا يساعد فقط في تخفيف الألم وفشل البطين الأيسر وارتفاع ضغط الدم الشرياني ، ولكنه يقلل أيضًا من حجم النخر والوفيات. يتم تحضير محاليل النترات للإعطاء عن طريق الوريد مؤقتًا: كل 10 ملغ من النتروجليسرين (على سبيل المثال ، 10 مل من محلول 0.1٪ على شكل بيرلينجانيت) أو ثنائي نترات إيزوسوربيد (على سبيل المثال ، 10 مل من محلول 0.1٪ على شكل من isoket) في 100 مل محلول فيسولوجي(20 ملغ من الدواء في 200 مل من محلول ملحي ، إلخ) ؛ وبالتالي 1 مل من المحلول المحضر يحتوي على 100 ميكروغرام ، وقطرة واحدة - 5 ميكروغرام من الدواء. تُعطى النترات بالتنقيط تحت السيطرة المستمرة على ضغط الدم ومعدل ضربات القلب بمعدل أولي من 5-10 ميكروغرام / دقيقة ، تليها زيادة في المعدل بمقدار 20 ميكروغرام / دقيقة كل 5 دقائق حتى يتحقق التأثير المطلوب أو أقصى معدل للإدارة 400 ميكروجرام / دقيقة. عادة ، يتحقق التأثير بمعدل 50-100 ميكروغرام / دقيقة. في حالة عدم وجود موزع ، يتم إعطاء المحلول المحضر المحتوي على 100 ميكروغرام من النترات في 1 مل تحت تحكم دقيق (انظر أعلاه) بمعدل أولي يبلغ 6-8 قطرات في الدقيقة ، والتي تخضع لديناميكا الدم المستقرة والحفاظ على الألم متلازمة ، يمكن زيادتها تدريجياً إلى الحد الأقصى - 30 نقطة في الدقيقة. يتم إدخال النترات من قبل فرق خطية ومتخصصة ويستمر في المستشفى. مدة إعطاء النترات في الوريد 24 ساعة أو أكثر ؛ 2-3 ساعات قبل نهاية التسريب ، يتم إعطاء الجرعة الأولى من النترات عن طريق الفم. جرعة زائدة من النترات تسبب انخفاض في النتاج القلبي وانخفاض ضغط الدم الانقباضي عن 80 ملم زئبق. الفن ، يمكن أن يؤدي إلى تدهور نضح الشريان التاجي وزيادة حجم احتشاء عضلة القلب.
لحل مشكلة إمكانية وصف النترات ، من الضروري توضيح عدد من النقاط:
- تأكد من أن ضغط الدم الانقباضي أعلى من 90 مم زئبق. فن. (للنيتروجليسرين قصير المفعول) أو أعلى من 100 مم زئبق. ش (لثنائي إيزوسوربيد ذو المفعول الأطول) ؛
- استبعاد وجود تضيق الأبهر واعتلال عضلة القلب الضخامي مع انسداد مجرى التدفق (تسمعيًا ووفقًا لبيانات مخطط كهربية القلب) ، وسكاك القلب (صورة سريرية للركود الوريدي في الدورة الدموية الجهازية مع الحد الأدنى من علامات فشل البطين الأيسر) والتهاب التامور الانقباضي (ثالوث بيك: ضغط وريدي مرتفع ، استسقاء ، "قلب هادئ صغير") ؛
- استبعاد ارتفاع ضغط الدم داخل الجمجمة وخلل الدورة الدموية الدماغي الحاد (بما في ذلك مظاهر السكتة الدماغية ، واعتلال الدماغ الحاد الناتج عن ارتفاع ضغط الدم ، وإصابات الدماغ الرضحية الحديثة) ؛
- استبعاد إمكانية الاستفزاز بالنترات لتطور متلازمة القذف المنخفض بسبب تلف البطين الأيمن في نوبة قلبية أو نقص تروية البطين الأيمن ، والذي قد يصاحب التوطين الخلفي (السفلي) لاحتشاء البطين الأيسر ، أو في الانصمام الخثاري الشريان الرئويمع تكوين القلب الرئوي الحاد.
- تأكد بمساعدة فحص الجس من عدم وجود ضغط مرتفع داخل العين (مع زرق انسداد الزاوية) ؛
- لتوضيح ما إذا كان المريض يعاني من عدم تحمل النترات.
ب. الحقن في الوريد لحاصرات بيتا
وكذلك استخدام النترات يساهم في تخفيف الآلام. إضعاف التأثيرات الودية على القلب (تتعزز هذه التأثيرات في أول 48 ساعة من احتشاء عضلة القلب بسبب المرض نفسه ونتيجة لرد الفعل على الألم) وتقليل الحاجة إلى أكسجين عضلة القلب ، فهي تساعد في تقليل حجم احتشاء عضلة القلب ، قمع عدم انتظام ضربات القلب البطيني ، وتقليل مخاطر تمزق عضلة القلب وزيادة طريقة بقاء المرضى على قيد الحياة. من المهم جدًا أن حاصرات بيتا ، وفقًا للبيانات التجريبية ، يمكن أن تؤخر موت الخلايا العضلية القلبية الإقفارية (فهي تزيد من الوقت الذي يكون خلاله تخثر الدم فعالاً).
في حالة عدم وجود موانع ، توصف حاصرات بيتا لجميع المرضى الذين يعانون من احتشاء عضلة القلب الحاد. في مرحلة ما قبل دخول المستشفى ، تكون مؤشرات إعطائهم عن طريق الوريد خاصة بالفريق الخطي - اضطرابات النظم المقابلة ، وبالنسبة للفريق المتخصص - متلازمة الألم المستمر ، وعدم انتظام دقات القلب ، وارتفاع ضغط الدم الشرياني. في أول 2-4 ساعات من المرض ، يشار إلى إعطاء بروبرانولول (obzidan) عن طريق الوريد الجزئي بمعدل 1 مجم في الدقيقة كل 3-5 دقائق تحت سيطرة ضغط الدم ومعدل ضربات القلب وتخطيط القلب حتى معدل ضربات القلب 55-60 تم الوصول إلى نبضة / دقيقة أو ما يصل إلى جرعات إجمالية قدرها 10 ملغ. في وجود بطء القلب ، علامات قصور القلب ، انسداد AV وانخفاض في ضغط الدم الانقباضي أقل من 100 ملم زئبق. فن. لا يوصف بروبرانولول ، ومع تطور هذه التغييرات على خلفية استخدامه ، يتم إيقاف إدارة الدواء.
لحل مشكلة إمكانية وصف حاصرات بيتا ، من الضروري توضيح عدد من النقاط:
- تأكد من عدم وجود قصور حاد في القلب أو فشل في الدورة الدموية في المرحلة الثانية والثالثة ، انخفاض ضغط الدم الشرياني ؛
- استبعاد وجود الحصار الأذيني البطيني ، الحصار الجيبي الأذيني ، متلازمة الجيوب الأنفية المريضة ، بطء القلب (معدل ضربات القلب أقل من 55 نبضة في الدقيقة) ؛
- استبعاد وجود الربو القصبي وأمراض الجهاز التنفسي الانسدادي الأخرى ، وكذلك التهاب الأنف الحركي الوعائي ؛
- استبعاد وجود أمراض الأوعية الدموية طمس (أو التهاب باطنة الشريان ، متلازمة رينود ، وما إلى ذلك) ؛
ج) التسريب الوريدي لكبريتات المغنيسيوم
يتم إجراؤه في المرضى الذين يعانون من نقص مغنسيوم الدم المؤكد أو المحتمل أو متلازمة QT الطويلة ، وكذلك في حالة مضاعفات احتشاء عضلة القلب مع بعض أنواع عدم انتظام ضربات القلب. في حالة عدم وجود موانع ، يمكن أن تعمل كبريتات المغنيسيوم كبديل محدد لاستخدام النترات وحاصرات بيتا ، إذا كان من المستحيل إدارتها لسبب ما (موانع أو غياب). وفقًا لنتائج عدد من الدراسات ، فإنه مثل الأدوية الأخرى التي تقلل من عمل القلب والطلب على الأكسجين لعضلة القلب ، تقلل الوفيات في احتشاء عضلة القلب الحاد ، كما تمنع تطور عدم انتظام ضربات القلب القاتلة (بما في ذلك إعادة ضخ الدم أثناء تخثر الدم الجهازي) و قصور القلب بعد الاحتشاء. في علاج احتشاء عضلة القلب الحاد ، يتم إعطاء 1000 مجم من المغنيسيوم (50 مل من 10 ٪ ، 25 مل من 20 ٪ أو 20 مل من 25 ٪ محلول كبريتات المغنيسيوم) عن طريق الوريد لمدة 30 دقيقة في 100 مل من محلول كلوريد الصوديوم متساوي التوتر ؛ بعد ذلك ، يتم إجراء التسريب بالتنقيط في الوريد خلال النهار بمعدل 100-120 مجم من المغنيسيوم في الساعة (5-6 مل من 10 ٪ ، 2.5-3 مل من 20 ٪ أو 2-2.4 مل من محلول 25 ٪ من كبريتات الماغنيسيوم).
لحل مشكلة مؤشرات تعيين كبريتات المغنيسيوم ، من الضروري توضيح عدد من النقاط:
- تحديد العلامات السريرية والشائنة لنقص مغنيسيوم الدم المحتمل - فرط الألدوستيرونية (بشكل أساسي في قصور القلب الاحتقاني وارتفاع ضغط الدم الأذيني المستقر) ، فرط نشاط الغدة الدرقية (بما في ذلك علاجي المنشأ) ، تسمم الكحول المزمن ، تقلصات العضلات المتشنجة ، الاستخدام طويل الأمد لمدرات البول ، علاج الجلوكوكورتيكويد ؛
- تشخيص وجود متلازمة فترة QT الطويلة بواسطة تخطيط كهربية القلب.
لحل مشكلة إمكانية وصف كبريتات المغنيسيوم ، من الضروري توضيح عدد من النقاط:
- تأكد من عدم وجود ظروف تتجلى في ارتفاع مغنيسيوم الدم - الفشل الكلوي ، الحماض الكيتوني السكري ، قصور الغدة الدرقية ؛
- استبعاد وجود الحصار الأذيني البطيني ، الحصار الجيبي الأذيني ، متلازمة الجيوب الأنفية المريضة ، بطء القلب (معدل ضربات القلب أقل من 55 نبضة في الدقيقة) ؛
استبعاد وجود الوهن العضلي الشديد في المريض ؛
- لتوضيح ما إذا كان المريض يعاني من عدم تحمل الدواء.
4. الحد من حجم احتشاء عضلة القلب
يتم تحقيقه عن طريق التخدير الكافي ، واستعادة تدفق الدم التاجي وانخفاض في عمل القلب والحاجة إلى الأكسجين في عضلة القلب.
يتم تقديم نفس الغرض عن طريق العلاج بالأكسجين ، المشار إليه في حالات احتشاء عضلة القلب الحاد في جميع المرضى بسبب التطور المتكرر لنقص الأكسجة في الدم ، حتى مع وجود مسار غير معقد للمرض. يُنصح باستنشاق الأكسجين المرطب ، إذا لم يسبب إزعاجًا مفرطًا ، باستخدام قناع أو من خلال قسطرة أنفية بمعدل 4-6 لتر / دقيقة خلال أول 24-48 ساعة من المرض (يبدأ في ما قبل- مرحلة المستشفى وتستمر في المستشفى).
5. العلاج والوقاية من مضاعفات احتشاء عضلة القلب.
جميع التدابير المذكورة أعلاه ، جنبًا إلى جنب مع توفير الراحة الجسدية والعقلية ، والاستشفاء على نقالة ، تعمل على منع مضاعفات احتشاء عضلة القلب الحاد. يتم إجراء العلاج في حالة تطورها بشكل تفاضلي اعتمادًا على متغير المضاعفات: الوذمة الرئوية ، والصدمة القلبية ، وعدم انتظام ضربات القلب واضطرابات التوصيل ، فضلاً عن نوبات الألم الطويلة أو المتكررة.
1). في فشل البطين الأيسر الحاد مع تطور الربو القلبي أو الوذمة الرئوية ، بالتزامن مع إدخال المسكنات المخدرة والنيتروجليسرين ، يتم حقن 40-120 مجم (4-12 مل) من محلول فوروسيميد (اللازكس) عن طريق الوريد ، الجرعة القصوى في مرحلة ما قبل دخول المستشفى 200 ملغ.
2). أساس علاج الصدمة القلبية هو الحد من منطقة الضرر وزيادة حجم عضلة القلب العاملة عن طريق تحسين تدفق الدم إلى مناطق نقص تروية القلب ، والتي يتم إجراء تخثر الدم الجهازي لها.
صدمة عدم انتظام ضربات القلب يتطلب استعادة فورية للإيقاع المناسب عن طريق إجراء العلاج بالنبضات الكهربائية ، والسرعة ، إذا كان من المستحيل إجراؤها ، يشار إلى العلاج الدوائي (انظر أدناه).
صدمة انعكاسية توقف بعد تسكين كاف. مع بطء القلب الأولي ، يجب أن يتم الجمع بين المسكنات الأفيونية والأتروبين بجرعة 0.5 مجم.
صدمة قلبية حقيقية (نوع ناقص الحركة من الدورة الدموية) بمثابة مؤشر ل أنا / الخامسالحقن بالتنقيط لعوامل غير مقوية للقلب (مؤثر في التقلص العضلي الإيجابي) - الدوبامين ، الدوبوتامين ، النوربينفرين. يجب أن يسبق ذلك تصحيح نقص حجم الدم. في حالة عدم وجود علامات لفشل البطين الأيسر الاحتقاني ، يتم تصحيح BCC عن طريق الحقن النفاث لمحلول كلوريد الصوديوم بنسبة 0.9 ٪ بحجم يصل إلى 200 مل في 10 دقائق مع تكرار إعطاء نفس الجرعة في حالة عدم وجود تأثير أو مضاعفات.
الدوبامين بجرعة 1-5 ميكروغرام / كغ / دقيقة له تأثير موسع للأوعية في الغالب ، 5-15 ميكروغرام / كغ / دقيقة - توسع الأوعية وتأثيرات مؤثر في التقلص العضلي الإيجابي ، 15-25 ميكروغرام / كغ / دقيقة - مؤثر في التقلص العضلي الإيجابي ( و chronotropic) وعمل تضيق الأوعية المحيطية. الجرعة الأولية هي 2-5 ميكروغرام / كغ / دقيقة مع زيادة تدريجية إلى الحد الأمثل.
لا يتسبب الدوبوتامين ، على عكس الدوبامين ، في توسع الأوعية ، ولكن له تأثير مؤثر في التقلص العضلي إيجابي قوي وزيادة أقل وضوحًا في معدل ضربات القلب وتأثير عدم انتظام ضربات القلب. يوصف الدواء بجرعة 2.5 ميكروجرام / كجم / دقيقة مع زيادة كل 15-30 دقيقة بمقدار 2.5 ميكروجرام / كجم / دقيقة حتى يتم الوصول إلى تأثير أو أثر جانبي أو جرعة 15 ميكروجرام / كجم / دقيقة.
يتم استخدام مزيج الدوبامين مع الدوبوتامين بالجرعات القصوى المسموح بها إذا كانت الجرعة القصوى لأحدهما لا تعمل أو إذا كان لا يمكن استخدام الجرعة القصوى من عقار واحد بسبب حدوث آثار جانبية (عدم انتظام دقات القلب الجيوب الأنفية أكثر من 140 في الدقيقة أو عدم انتظام ضربات القلب البطيني).
مزيج من الدوبامين أو الدوبوتامين مع النوربينفرين بجرعة 8 ميكروغرام / دقيقة.
يتم استخدام Norepinephrine (norepinephrine) كعلاج أحادي عندما يكون من المستحيل استخدام أمينات الضغط الأخرى. يوصف بجرعة لا تتجاوز 16 ميكروغرام / دقيقة ، بالاشتراك مع تسريب من النتروجليسرين أو ثنائي نترات إيزوسوربيد بمعدل 5-200 ميكروغرام / دقيقة.
3). قد يكون الانقباض البطيني في المرحلة الحادة من احتشاء عضلة القلب نذير رجفان بطيني. يُعطى الدواء المختار لعلاج عدم انتظام ضربات القلب البطيني - ليدوكائين - عن طريق الوريد على شكل بلعة بمعدل 1 مجم / كجم من وزن الجسم ، يليها حقنة بالتنقيط من 2-4 مجم / دقيقة. لا ينصح بالإعطاء الوقائي المستخدم لليدوكائين لجميع المرضى الذين يعانون من احتشاء عضلة القلب الحاد (يزيد الدواء من الوفيات بسبب توقف الانقباض). مرضى قصور القلب الاحتقاني أمراض الكبدتدار بجرعة نصف.
بالنسبة لتسرع القلب البطيني والرفرفة الأذينية والرجفان الأذيني مع ارتفاع معدل ضربات القلب وعدم استقرار الدورة الدموية ، فإن إزالة الرجفان هي العلاج المفضل. مع عدم انتظام ضربات القلب الأذيني وديناميكا الدم المستقرة ، يستخدمون (أنابريلين ، أوبزيدان) لإبطاء معدل ضربات القلب.
مع تطور الكتلة الأذينية البطينية من الدرجة الثانية إلى الثالثة ، يتم إعطاء 1 مل من محلول الأتروبين 0.1٪ عن طريق الوريد ، مع عدم فعالية العلاج التجريبي بالأتروبين وظهور الإغماء (هجمات Morgagni-Edems-Stokes) ، يشار إلى سرعة مؤقتة .
أخطاء العلاج الشائعة.
يستلزم ارتفاع معدل الوفيات في الساعات والأيام الأولى من احتشاء عضلة القلب تعيين علاج دوائي مناسب ، بدءًا من الدقائق الأولى للمرض. يؤدي ضياع الوقت إلى تفاقم الإنذار بشكل كبير.
ج: أخطاء ناتجة عن توصيات قديمة ، محفوظة جزئيًا في بعض المعايير الحديثة للرعاية الطبية في مرحلة ما قبل دخول المستشفى.
الخطأ الأكثر شيوعًا هو استخدام مخطط من ثلاث مراحل للتخدير: في حالة عدم وجود تأثير إعطاء النتروجليسرين تحت اللسان ، لا يتم الانتقال إلى المسكنات المخدرة إلا بعد محاولة فاشلة لوقف متلازمة الألم باستخدام مزيج مسكن غير مخدر(ميتاميزول الصوديوم - أنالجين) مع مضادات الهيستامين (ديفينيدرامين - ديميدرول). وفي الوقت نفسه ، فإن ضياع الوقت عند استخدام مثل هذه المجموعة ، والتي ، كقاعدة عامة ، لا تسمح بذلك مكتملالمسكنات ، وثانياً ، ليست قادرة ، على عكس المسكنات المخدرة ، على توفيرها تفريغ الدورة الدموية للقلب(الهدف الرئيسي للتخدير) وتقليل الطلب على الأكسجين لعضلة القلب ، يؤدي إلى تفاقم الحالة وتكهن أسوأ.
في كثير من الأحيان أقل بكثير ، ولكن لا تزال تستخدم مضادات التشنج العضلي (كاستثناء ، يتم استخدام بابافيرين الموصى به سابقًا ، والذي تم استبداله بـ drotaverine - no-shpa) ، والتي لا تحسن نضح المنطقة المصابة ، ولكنها تزيد من طلب الأكسجين في عضلة القلب.
من غير المناسب استخدام الأتروبين للوقاية (وهذا لا ينطبق على التخفيف) من تأثيرات المورفين (الغثيان والقيء والتأثيرات على معدل ضربات القلب وضغط الدم) ، لأنه يمكن أن يزيد من عمل القلب.
إن الإعطاء الوقائي الموصى به لليدوكائين لجميع المرضى الذين يعانون من احتشاء عضلة القلب الحاد دون مراعاة الوضع الحقيقي ، ومنع تطور الرجفان البطيني ، يمكن أن يزيد بشكل كبير من الوفيات بسبب بداية توقف الانقباض.
ب- أخطاء ناجمة عن أسباب أخرى.
في كثير من الأحيان ، لغرض تخفيف الآلام في الحالة الوعائية ، يتم استخدام عقار ميتاميزول الصوديوم المركب مع بروميد الفينبيرين وهيدروكلوريد بيتوفينون (بارالجين ، سباسمالجين ، سبازجان ، إلخ) بشكل غير مبرر ، والذي لا يؤثر عمليًا على الأداء الوظيفي من استهلاك القلب والأكسجين لعضلة القلب ، وبالتالي لا يظهر في هذه الحالة (انظر أعلاه).
من الخطير للغاية في حالة احتشاء عضلة القلب أن تستخدم كعامل مضاد للصفيحات و dipyramole "التاجي" (الدقات) ، مما يزيد بشكل كبير من طلب الأكسجين في عضلة القلب.
خطأ شائع جدًا هو تعيين أسبارتات البوتاسيوم والمغنيسيوم (أسباركام ، بانانجين) ، والذي لا يؤثر على العمل الخارجي للقلب ، أو استهلاك الأكسجين لعضلة القلب ، أو تدفق الدم التاجي ، إلخ.
استطبابات.
احتشاء عضلة القلب الحاد هو مؤشر مباشر للدخول إلى المستشفى في وحدة العناية المركزة (كتلة) أو تنشيط القلب. يتم النقل على نقالة.
ما هو احتشاء عضلة القلب؟ يدخل الدم إلى القلب عبر الشرايين التاجية. يمكن أن يترسب الكوليسترول على جدرانها ، مما يؤدي إلى تضييق الأوعية الدموية وتشكيل ما يسمى اللويحات. تسمى هذه العملية تصلب الشرايين ويمكن أن تستغرق عقودًا. إذا تم تدمير اللويحة ، تبدأ جلطة دموية في التكون في مكانها ، مما يقلل من تدفق الدم إلى القلب. إذا أدت الجلطة الدموية إلى انسداد الشريان التاجي بشكل كامل أو شبه كامل ، تحدث نوبة قلبية. خلايا القلب لا تتلقى الدم ومعه الأكسجين ، وتبدأ في الموت. كلما مر الوقت من لحظة انتهاك تدفق الدم إلى بدء العلاج ، كلما زاد الضرر.
انتباه! عند أدنى شك في حدوث نوبة قلبية ، اتصل على الفور سياره اسعاف: عامل الوقت حاسم في مسألة إنقاذ حياة الضحية وقدرتها على العمل.
تعرف على الأعراض
 تختلف علامات احتشاء عضلة القلب باختلاف الأشخاص ، كما يمكن أن تختلف شدة المظاهر. يعاني البعض من نوبة قلبية ، كما يقولون ، "على أقدامهم" ، بينما لا يعانون من الألم على الإطلاق. ولكن في معظم الحالات ، تكون أول علامة على الإصابة بنوبة قلبية ألم شديد في الصدر. يصف الكثيرون هذا الألم بأنه ضغط ، وضغط ، وشعور بالامتلاء في الصدر. يمكن أن ينتشر الألم إلى الظهر والذراع الأيسر والعنق والفك وأعلى البطن وأحيانًا إلى الذراع اليمنى. قد تكون دائمة ، أو تمر بعد بضع دقائق ثم تستأنف.
تختلف علامات احتشاء عضلة القلب باختلاف الأشخاص ، كما يمكن أن تختلف شدة المظاهر. يعاني البعض من نوبة قلبية ، كما يقولون ، "على أقدامهم" ، بينما لا يعانون من الألم على الإطلاق. ولكن في معظم الحالات ، تكون أول علامة على الإصابة بنوبة قلبية ألم شديد في الصدر. يصف الكثيرون هذا الألم بأنه ضغط ، وضغط ، وشعور بالامتلاء في الصدر. يمكن أن ينتشر الألم إلى الظهر والذراع الأيسر والعنق والفك وأعلى البطن وأحيانًا إلى الذراع اليمنى. قد تكون دائمة ، أو تمر بعد بضع دقائق ثم تستأنف.
فيما يلي قائمة بالأعراض الرئيسية:
- ألم ضغط مفاجئ أو ضغط في منتصف الصدر يستمر لعدة دقائق أو أكثر ؛
- يمكن أن ينتشر الألم نصل الكتف الأيسروالذراع الأيسر أو الرقبة أو الفك.
- ممكن حرقة أو ألم مستمرفي منطقة المعدة.
- صعوبة في التنفس وضيق في التنفس.
- الدوخة أو الإغماء.
- الضعف أو الشعور بالتعب.
- التعرق الغزير؛
- قشعريرة.
- آلام الظهر.
- خدر في الذراع أو الفك.
- الهياج والقلق والأرق والخوف من الموت.
- شحوب،
- شفاه وأذنان زرقاء وأطراف الأصابع.
شعر الكثير ممن أصيبوا بنوبة قلبية بألم في الصدر وضيق في التنفس وضعف في الأيام التي سبقت النوبة. بالنسبة للبعض ، فإن النوبة القلبية يسبقها عدم انتظام ضربات القلب (اضطراب ضربات القلب). على عكس نوبة الذبحة الصدرية ، لا يقلل النتروجليسرين من ألم النوبة القلبية. عادة ما تكون نوبة الألم نفسها أطول وأقوى من الذبحة الصدرية. في حالات نادرة جدًا ، يمكن أن تكون النوبة القلبية بدون أعراض ويتم اكتشافها بالصدفة في مخطط كهربية القلب المأخوذ لسبب آخر.
يتجاهل البعض الأعراض أو ينسبونها إلى حالة أخرى ، مثل عسر الهضم أو عدوى معوية. ولكن نظرًا لأن معظم الوفيات تحدث في غضون ساعة من ظهور الأعراض الأولى ، فمن الضروري التعرف على النوبة القلبية في الوقت المناسب والعمل بسرعة. فكلما بدأ العلاج مبكرًا ، قل وقت موت خلايا القلب وكلما كان ذلك أفضل. التكهن على المدى الطويل.
تحذير خاص بالمرأة
يعاني الأشخاص المختلفون من نوبة قلبية بطرق مختلفة ، لكن تنوع الأعراض لدى النساء أعلى في المتوسط. بالإضافة إلى ذلك ، لدى النساء أعلى عتبة الألم(تحمل الألم بسهولة أكبر). قد تكون أعراضهم الرئيسية هي الغثيان والدوار والضعف والتعرق ، لون ازرقالشفاه والأظافر والأرق.
ما يجب القيام به
عند أدنى شك في حدوث نوبة قلبية ، اتصل بالطبيب. حتى لو لم يكن هناك يقين من أنه هو ، فمن الأفضل أن تكون آمنًا من تأخير العلاج. تعتمد الحياة على مدى سرعة تقديم المساعدة.
- في الأعراض الأولى ، الجلوس ، أو بالأحرى الاستلقاء ؛
- إذا استمرت الأعراض لأكثر من ثلاث دقائق ، اتصل بسيارة إسعاف ، وأخبر المرسل أنك تعاني من نوبة قلبية ؛
- إذا كان لديك أقراص نيتروجليسرين ، خذ ثلاث مرات مرة واحدة بفاصل 5 دقائق (لا تفعل هذا إذا كان الوجه شاحبًا ، فهناك "ذباب" أمام العينين والرأس يدور: قد يكون هذا علامة على الضغط المنخفض ، والذي "ينخفض" النتروجليسرين أكثر) ؛
- إذا لم يكن لديك نيتروجليسرين ، فتناول الأسبرين: فهو يقلل الجلطات الدموية.
- غط نفسك بشيء دافئ إذا كنت ترتجف ؛
- لا تحاول أن تقود سيارتك إلى المستشفى بمفردك ، ناهيك عن القيادة.
الإنعاش القلبي
يمكن أن ينقذ حياة إذا تم تدريب أقارب المريض على هذه التقنية. يمكن للأشخاص الذين ليس لديهم خلفية طبية تعلمها في دورات الإسعافات الأولية.

يشمل الإنعاش القلبي الرئوي تهوية صناعيةضغطات الرئة والصدر. نظرًا لأن هذا قد يتسبب في إصابة خطيرة ، فلا تتذكر ما شاهدته في الأفلام وحاول وضعه موضع التنفيذ. قبل البدء في الإنعاش القلبي الرئوي ، تحتاج إلى استدعاء سيارة إسعاف ولا توقف الإجراء حتى وصوله.
يجب تدريب أقارب مرضى الذبحة الصدرية على هذه التقنية. توجد دورات تدريبية بدعم من الصليب الأحمر في العديد من المدن ، ويمكنك معرفة ما إذا كانت موجودة في مدينتك على الموقع الإلكتروني لهذه المنظمة. تقدم العديد من الشركات التجارية تدريبات مماثلة. أما بالنسبة للتعلم عن بعد ، فإن فعاليته مشكوك فيها ، لأنه من المستحيل اتخاذ الإجراءات اللازمة في الممارسة العملية.
الرجفان

 قد يكون جهاز إزالة رجفان القلب القابل للزرع مفيدًا للأشخاص الذين يعانون من عدم انتظام دقات القلب البطيني أو نوبات الخفقان. عندما تحدث مثل هذه الحالات ، فإنها تنتج تفريغًا كهربائيًا يعيد الإيقاع الطبيعي للقلب. كما أنه يحفز عمل القلب أثناء توقفه المفاجئ.
قد يكون جهاز إزالة رجفان القلب القابل للزرع مفيدًا للأشخاص الذين يعانون من عدم انتظام دقات القلب البطيني أو نوبات الخفقان. عندما تحدث مثل هذه الحالات ، فإنها تنتج تفريغًا كهربائيًا يعيد الإيقاع الطبيعي للقلب. كما أنه يحفز عمل القلب أثناء توقفه المفاجئ.
على الرغم من حقيقة أن الجهاز يستخدم بنشاط في الدول الغربية ، إلا أنه لا توجد حتى الآن طريقة دقيقة لاختيار المرضى الذين يعانون من مؤشرات للزرع. في بلدنا ، يتم إجراء مثل هذه العمليات ، ويمكن الحصول على معلومات أكثر تحديدًا من طبيب القلب. نظرًا لأن مثل هذا الإجراء لا يمكن وصفه لنفسه بمفرده ، فستكون هناك حاجة للتشاور مع طبيب القلب في أي حال.
لا يمكن أن يكون جهاز إزالة رجفان القلب المحمول فعالاً إلا في يد شخص يعرف كيفية استخدامه. ليس من الصعب شرائه ، بما في ذلك عبر الإنترنت ، ولكن مع التدريب ، يكون كل شيء أكثر تعقيدًا. لكي نفهم كيف تسير الأمور مع هذا في بلدنا ، يكفي أن نذكر أن عيادات الدولة غير مجهزة بهذه الأجهزة. ومع ذلك، في طارئيمكن لجهاز إزالة رجفان القلب أن ينقذ الحياة ، ويأتي الكثير منها بتعليمات بسيطة وواضحة.

ولكن ، كما تظهر الممارسة ، فإن أصعب شيء في وقت الإصابة بنوبة قلبية بالنسبة للضحية ومن حوله هو عدم الذعر والحفاظ على القدرة على القيام بأفعال ذات مغزى.
بالنسبة لاحتشاء عضلة القلب - وهو شكل حاد من أمراض القلب التاجية (CHD) - يتميز بتطور النخر الموضعي (النخر) في عضلة القلب. يعود سبب موت أنسجة عضلة القلب إلى عجز مطلق أو قصور نسبي في إمداد الدم في هذه المنطقة. تسمح طرق البحث الحديثة بتشخيص حالة حرجة المرحلة الأوليةويفرق بين احتشاء عضلة القلب والأمراض الأخرى ذات الأعراض المماثلة.
وصف
يحدث احتشاء في الطبقة العضلية السميكة للقلب (عضلة القلب) بسبب انسداد الشريان التاجي
يحدث احتشاء عضلة القلب بسبب انسداد الشريان التاجي - الأوعية الدموية التي تغذي عضلة القلب. العامل المثير الرئيسي في حدوث أزمة حادة هو تصلب الشرايين - ترسبات على جدران مجرى الدم على شكل لويحات كولسترول.
تشمل الأسباب الرئيسية للاضطرابات الإقفارية ما يلي:
- كبار السن؛
- التدخين؛
- تلف صمامات القلب.
- اعتلال عضلة القلب.
- زيادة في تركيز الدهون والفيبرينوجين في البلازما.
- وجود صمام قلب اصطناعي.
- التهاب الشغاف الجرثومي.
- كثرة الصفيحات.
- تخثر وريدي.
يمثل الهيكل التشريحي للقلب بطينين وأذينين ، ولكن غالبًا ما يتم ملاحظة هزيمة النوبة القلبية في عزلة في البطين الأيسر. نادرًا ما يتم تسجيل الأضرار المستقلة للأذينين والبطين الأيمن.
على الأكثر اعراض شائعةيشمل:
- حرقان في منطقة الصدر;
- الشعور بالثقل في منطقة الرقبة.
- عدم الراحة في منطقة الفك.
- ضعف العضلات
- ضيق في التنفس
- صعوبة في التنفس
- عدم انتظام ضربات القلب.
السمات المميزة لهجوم الألم في احتشاء عضلة القلب
| ميزة الحجز | صفة مميزة |
| توطين الألم | خلف القص ، في كثير من الأحيان في منطقة القلب |
| طبيعة الألم | الضغط والعصر والحرق وآلام القطع |
| موقف المريض | يتجمد في مكانه - يخشى القيام بأي حركة بسبب زيادة الألم |
| سلوك المريض | القلق والخوف والقلق |
| تشعيع الآلام | في الكتف الأيسر ، الذراع الأيسر ، النصف الأيسر من العنق والرأس ، تحت نصل الكتف الأيسر |
| مدة الهجوم | نوبة الألم طويلة الأمد ، ولا تزول عن طريق تناول النتروجليسرين أو يمر لفترة قصيرة وتعاود الظهور |
كل مريض خامس يصاب بنوبة قلبية دون حدوث أعراض مرضية.
طرق التشخيص ومؤشراتها حسب مرحلة احتشاء عضلة القلب
في حالة الاشتباه في احتشاء عضلة القلب ، يجب إجراء الدراسات التشخيصية التالية على وجه السرعة:
- فحص الدم (عام ، الكيمياء الحيوية) ؛
- تخطيط كهربية القلب (ECG) ؛
- تخطيط صدى القلب (EchoCG).
الأحداث المؤجلة هي:
- تصوير الأوعية التاجية - طريقة لفحص القلب بعامل تباين ؛
- التصوير الومضاني هو طريقة لتشخيص النويدات المشعة.
يمر احتشاء عضلة القلب في تطوره بأربع مراحل ، يتميز كل منها بأعراضه الخاصة:
- المرحلة 1 - المرحلة الأكثر حدة من الضرر ، تستمر من لحظة البداية حالة حرجةقبل تطور الآفات النخرية. تتراوح المدة من عدة ساعات إلى ثلاثة أيام.
- المرحلة 2 - حاد ، لوحظ في الفترة الفاصلة من نقطة تطور التغيرات النخرية إلى وقت استقرار العملية. مدته تتراوح من بضعة أيام إلى ثلاثة أسابيع.
- المرحلة 3 - تحت الحاد ، تتميز بانخفاض في منطقة الآفة ، والحد من منطقة النخر ، وظهور تندب الشريان التاجي. يمكن أن تستمر هذه المرحلة لمدة تصل إلى ثلاثة أشهر.
- المرحلة 4 - مرحلة الندبات (تستغرق من 4-8 أسابيع إلى ثمانية أشهر).
فحص الدم العام
تشير التغييرات التالية في تكوين الدم إلى احتشاء عضلة القلب.
- زيادة عدد الكريات البيضاء. بضع ساعات أو خلال اليوم الأول بعد حالة حادة ، لوحظ زيادة عدد الكريات البيضاء - زيادة في اللون الأبيض خلايا الدم- الكريات البيض. تتراوح القيم الطبيعية للأشخاص الذين تزيد أعمارهم عن 16 عامًا من 4-9 × 10 * 9 / لتر. مع نوبة قلبية ، يرتفع عددهم إلى 10-15 × 10 * 9 / لتر.يعود المؤشر إلى طبيعته بعد 3-4 أيام.
- تحول صيغة الكريات البيض. بعد بضع ساعات ، في صيغة الكريات البيض (النسبة المئوية لأنواع الكريات البيض الموجودة) ، يتم تحديد تحول كبير إلى اليسار.
- زيادة في الحمضات. في اليوم الخامس إلى السابع (في المرحلة الثانية) ، تم إصلاح فرط الحمضات - زيادة في الخلايا البلعمية. عادة ، في الأطفال والبالغين ، بغض النظر عن الجنس ، المحتوى النسبي للحمضات يتراوح من 1-5٪ ، العدلات - 80٪ ، طعنة العدلات - 12٪.
- زيادة العائد على حقوق الملكية. يظل معدل ترسيب كرات الدم الحمراء (ESR) دون تغيير في اليوم الأول. المؤشرات الطبيعية للذكور هي 2-10 مم / ساعة ، للنساء - 3-15 مم / ساعة.بعد هذا المقطع ، يمكن أن تزيد ESR وتستمر حتى 40 يومًا.
كيمياء الدم
الطريقة الأكثر إفادة هي اختبار الدم الكيميائي الحيوي للبروتينات القلبية - علامات تلف عضلة القلب ، والتي ترد خصائصها الرئيسية في الجدول.
| فِهرِس | وقت تثبيت العلامة في الدم | قيمة الذروة | مدة العودة إلى وضعها الطبيعي | ملحوظة |
| تروبونين تي | 2.5 - 3 ساعات | الذروة الأولى - 10 ساعات ؛ الذروة الثانية - 96 ساعة | حتى 20 يومًا | تشير الزيادة في تروبونين تي في حدود عالية (تصل إلى 400 مرة طبيعية) إلى احتشاء كبير البؤرة أو عبر الجافية. تشير الزيادة في المؤشر بما لا يزيد عن 37 مرة إلى حدوث احتشاء عضلة القلب بدون موجة Q. ولا يتجاوز المستوى الطبيعي لتروبونين تي في دم الشخص السليم 0.5 نانوغرام / مل. |
| تروبونين الأول | ساعاتين | الذروة الأولى - 6 ساعات ، كحد أقصى - يومين | تصل إلى 7 أيام | عادة لا يتم الكشف عن تروبونين 1. عند تفسير نتائج التروبونين الأول الذي أدرسه ، يجب أن يؤخذ في الاعتبار أن الميزة التفاضلية بين احتشاء عضلة القلب والأمراض الأخرى هي تركيز العلامة في قيم 2-2.5 نانوغرام / مل. |
| الميوغلوبين | 30 دقيقة | من 6 إلى 12 ساعة | من 12 إلى 24 ساعة | أحد مؤشرات احتشاء عضلة القلب هو زيادة الميوجلوبين بنسبة 15-20 مرة. تتراوح القيمة المرجعية لمركبات البروتين هذه من 22 إلى 66 ميكروجرام / لتر للرجال و21 إلى 49 ميكروجرام / لتر للنساء. |
| CPK (الكرياتين كيناز) إجمالي | من 6 إلى 12 ساعة | بعد 12-24 ساعة | تصل إلى 4 أيام | الزيادة المتوقعة في الكرياتين كيناز هي 3-30 مرة. القاعدة: للنساء - أقل من 167 وحدة / لتر ، للرجال - أقل من 190 وحدة / لتر. |
| CPK (فوسفوكيناز الكرياتين) MB | 3 ساعات | 12 ساعة | لمدة 3-6 أيام | معيار CPK-MB: أقل من 24 وحدة / لتر ، وأقل من 6٪ من مستوى نشاط CPK. تشير الزيادة في القيم إلى حدوث بؤرة نخر في عضلة القلب. |
للحصول على معلومات! عند تأكيد الإصابة باحتشاء عضلة القلب ، يوصى بإجراء اختبار الدم البيوكيميائي بشكل متكرر.
تخطيط القلب الكهربي
تعد طريقة تخطيط القلب طريقة غير مكلفة نسبيًا تسمح لك بتسجيل وتقييم وظائف القلب بيانياً في لحظة معينةوقت. يتم تسجيل الإشارات الكهربائية المنبعثة من عمل القلب باستخدام أقطاب كهربائية موضوعة في نقاط قياسية بالجسم ومتصلة بجهاز تخطيط القلب. لا يسمح مخطط كهربية القلب (ECG) فقط باستبعاد أو تأكيد احتشاء عضلة القلب ، ولكن أيضًا لتحديد موقع الآفة ، وحجم وعمق التغيرات النخرية ، لتحديد مرحلة الحالة الحرجة ووجود المضاعفات.
بفضل مخطط كهربية القلب (ECG) ، من الممكن تحديد موضع الآفة ، وكذلك تحديد مرحلة الحالة الحرجة
القيم الرسومية لتخطيط القلب غير متسقة. تتقلب حسب مرحلة الاحتشاء. العلامات التشخيصية لنخر عضلة القلب هي:
- ارتفاع مقوس للجزء ST فوق العزل مع انتفاخ لأعلى في مرحلة مبكرة ؛
- تشكيل موجة Q غير طبيعية (QS) ؛
- تشكيل موجة T متناظرة سلبية عميقة ؛
- الاستبدال المحتمل لـ QS بمركب Qr أو QR ؛
- في المرحلة الرابعة ، يقع الجزء ST على العزلة ؛
- في المرحلة النهائية ، يكون اتساع الموجة T أقل وضوحًا.
تختلف علامات مخطط كهربية القلب تبعًا لمرحلة احتشاء عضلة القلب
كما أن مخطط كهربية القلب يجعل من الممكن تمييز موضع النوبة القلبية.
يتيح تخطيط القلب أيضًا تحديد موضع احتشاء عضلة القلب.
تخطيط صدى القلب
يمكن لتخطيط صدى القلب تأكيد أو دحض احتشاء عضلة القلب الحاد لدى الأفراد الذين يعانون من احتشاء عضلة القلب على المدى الطويل ألمفي منطقة الصدر. بالإضافة إلى ذلك ، وفقًا لنتائج تخطيط صدى القلب ، يمكنك:
- تقييم مدى الضرر الذي يصيب عضلة القلب وتحديد منطقة الانتهاكات ؛
- تحديد الحجم الحقيقي للآفة بعد العلاج ؛
- تحديد المرضى الذين يعانون من معلمات الدورة الدموية غير المستقرة ؛
- تحديد وتقييم المضاعفات ؛
- تحليل حيوية عضلة القلب.
- لفحص وظائف البطينين الأيمن والأيسر ؛
- تصور الأزمات التي مر بها المريض في وقت سابق ؛
- توقع نتيجة المرض.
تخطيط صدى القلب هو وسيلة التشخيص الرائدة للتمييز بين مضاعفات عضلة القلب
وميض
يتم إجراء التصوير الومضاني لتأكيد التشخيص وتقييم حجم تلف عضلة القلب. تسمح الصور الناتجة بتصور قدرات انقباض عضلة القلب في وضع التصوير المقطعي.
التصوير الومضاني هو طريقة عالية الدقة لتحديد فعالية العلاج الدوائي والعمليات الجراحية التي يتم إجراؤها: رأب الأوعية التاجية باستخدام الدعامة ، وتطعيم المجازة التاجية.
تتيح لك هذه الطريقة التحكم في برامج إعادة التأهيل المستمرة ، فضلاً عن إجراء التعديلات اللازمة عليها.
تصوير الأوعية التاجية
يستخدم تصوير الأوعية التاجية (CAG) في حالة وجود أعراض سريرية مشكوك فيها وغياب العلامات التشخيصية على مخطط كهربية القلب. تسمح لك الدراسة بتحديد الانخفاض في سالكية الشريان التاجي بدقة ، والتفريق بين احتشاء عضلة القلب والأمراض الحادة الأخرى.
الأشعة السينية الصدر
يسمح التصوير الشعاعي بالتفريق بين احتشاء عضلة القلب وأمراض الرئة. بمساعدة هذه الدراسة ، يمكن للطبيب تحديد فشل القلب في البطين الأيسر. تعتبر طريقة التشخيص هذه ضرورية لزيادة خطر تشريح تمدد الأوعية الدموية الأبهري.
يعتبر احتشاء عضلة القلب من أكثر حالات احتشاء عضلة القلب عواقب وخيمةمرض القلب الإقفاري. إذا كانت لديك أي أعراض مشبوهة ، فاتصل بطبيبك على الفور. يسمح التشخيص التفريقي في الوقت المناسب باختيار استراتيجية العلاج الصحيحة والوقاية من المضاعفات الخطيرة.
37593 0
في عام 2005 ، اقترح خبراء مجموعة العمل التابعة لجمعية القلب البريطانية تصنيفًا جديدًا لمتلازمات الشريان التاجي الحادة (ACS):
1. ACS مع الذبحة الصدرية غير المستقرة (لم يتم تحديد العلامات البيوكيميائية للنخر) ؛
2. ACS مع نخر عضلة القلب (تركيز تروبونين T أقل من 1.0 نانوغرام / مل أو تركيز تروبونين 1 (اختبار AccuTnI) أقل من 0.5 نانوغرام / مل ؛
3. ACS مع علامات سريرية لاحتشاء عضلة القلب (MI) مع تروبونين Ti .0 نانوغرام / مل أو تروبونين 1 (اختبار AccuTnI)> 0.5 نانوغرام / مل.
هناك العديد من تصنيفات احتشاء عضلة القلب اعتمادًا على التغييرات الأولية في مخطط كهربية القلب ، أو توطين بؤرة نخر عضلة القلب ، أو اعتمادًا على وقت تطور علم الأمراض.
اعتمادًا على توقيت البداية وطبيعة مسار علم الأمراض ، هناك:
- MI الابتدائية ؛
- متكرر MI
- كرر MI.
اعتمادًا على التغييرات الأولية في مخطط كهربية القلب ، هناك:
- احتشاء عضلة القلب دون ارتفاع الجزء ST ؛
- ارتفاع المقطع ST MI بدون موجة Q المرضية ؛
- ارتفاع ST MI مع موجة Q غير طبيعية.
اعتمادًا على مدى وتوطين بؤرة النخر ، هناك:
- مي بؤري صغير ؛
- MI بؤري كبير ؛
- عبر مي
- دائري (تحت الشغاف) ؛
- MI للجدار الأمامي للبطين الأيسر.
- MI للجدار الجانبي للبطين الأيسر ؛
- MI للجدار الخلفي للبطين الأيسر ؛
- MI للجدار السفلي للبطين الأيسر (الحجاب الحاجز) ؛
- MI للبطين الأيمن.
معايير التشخيص لـ MI:
- وجود ألم نموذجي للذبحة الصدرية خلف عظمة القص ("ألم إقفاري") يستمر لأكثر من 30 دقيقة ؛
- تغييرات نموذجية في تخطيط القلب ؛
- زيادة في تركيز علامات تلف الخلايا العضلية في الدم (الميوغلوبين ؛ تروبونين - TnI ، TnT ؛ CPK - جزء MB ؛ Transaminases - AST / ALT ؛ نازعة هيدروجين اللاكتات).
لإجراء تشخيص "احتشاء عضلي" "معين" ، يجب أن يكون هناك 2 من المعايير الثلاثة المذكورة أعلاه.
الصورة السريرية لاحتشاء عضلة القلب
تم وصف العلامات السريرية الكلاسيكية لـ AMI بواسطة J.B. Herrick في عام 1912: ألم ضيق في منطقة الصدر الواقعة خلف القص ، وغالبًا ما يرتبط بالانتشار إلى الرقبة أو الذراع أو الظهر (منطقة بين القطبين) لمدة تزيد عن 30 دقيقة ، مما يتطلب إعطاء مواد أفيونية للتخفيف. غالبًا ما كان الألم مصحوبًا بضيق في التنفس والغثيان والقيء والإغماء ومشاعر الموت الوشيك. ومع ذلك ، قد تكون هذه العلامات السريرية في بعض الحالات غائبة أو معدلة ، وقد يسبق القلق ظهور الألم خلف القص (الأعراض البادرية).
تتنوع الصورة السريرية لـ MI ، ووفقًا لوجود الأعراض وطبيعة الشكاوى ، يتم تمييز المتغيرات السريرية لظهور المرض.
- البديل الزاوي- ألم ضغط حاد نموذجي خلف القص ، يستمر لأكثر من 30 دقيقة ولا يتوقف عن طريق تناول أقراص أو رذاذ من النترات العضوية. غالبًا ما ينتشر الألم إلى النصف الأيسر من الصدر والفك السفلي والذراع الأيسر أو الظهر ، مصحوبًا بالقلق والخوف من الموت والضعف والتعرق الغزير. يحدث مجمع الأعراض هذا في 75-90٪ من الحالات.
- متغير الربو- الضرر الإقفاري للقلب يتجلى في ضيق التنفس ، ضيق التنفس ، خفقان القلب. عنصر الألم غائب أو ضعيف التعبير. ومع ذلك ، مع الاستجواب الدقيق للمريض ، يمكن الكشف عن أن الألم سبق تطور ضيق التنفس. يتم تسجيل تواتر هذا المتغير السريري من MI في 10 ٪ بين المرضى من الفئة العمرية الأكبر ومع تكرار MI.
- البديل المعدي (البطن)- الألم موضعي في مناطق النصف العلوي من البطن ، عملية الخنجري ، غالبًا ما تشع في الفضاء بين القطبين ، وكقاعدة عامة ، يتم دمجها مع اضطرابات عسر الهضم (الفواق ، التجشؤ ، الغثيان ، القيء) ، أعراض انسداد معوي ديناميكي (انتفاخ ، ضعف ضوضاء قرع). غالبًا ما يحدث المتغير المعدي مع انخفاض MI ولا يتجاوز 5 ٪ من جميع حالات كارثة القلب.
- متغير عدم انتظام ضربات القلب- الشكوى الرئيسية هي الشعور بـ "التلاشي" ، الانقطاعات في عمل القلب ، الخفقان ، المصحوب بتطور ضعف شديد ، إغماء أو أعراض عصبية أخرى ، بسبب تدهور الدورة الدموية الدماغية على خلفية انخفاض الدم ضغط. الألم غائب أو لا يجذب انتباه المريض. يتراوح تواتر متغير عدم انتظام ضربات القلب من 1-5٪ من الحالات.
- البديل الدماغي الوعائي- دوار ، توهان ، إغماء ، غثيان وقيء من مصدر مركزي ، ناتج عن نقص التروية الدماغية. سبب تدهور الدورة الدموية الدماغية هو انتهاك وظيفة ضخ القلب مع انخفاض في الدم على خلفية عدم انتظام ضربات القلب (عدم انتظام ضربات القلب) أو جرعة زائدة من النترات. تزداد نسبة حدوث احتشاء عضلة القلب الدماغية مع تقدم العمر وتتراوح من 5 إلى 10٪ من العدد الإجمالي للمرض.
- البديل بدون أعراض- كشف MI في دراسة تخطيط القلبومع ذلك ، في تحليل بأثر رجعي لتاريخ المرض في 70-90٪ من الحالات ، يشير المرضى إلى ضعف سابق غير محفز ، أو تدهور في المزاج ، أو ظهور عدم راحة في الصدر أو زيادة في نوبات الذبحة الصدرية مصحوبة بضيق في التنفس ، انقطاعات في القلب. هذا النوع السريري من MI هو الأكثر شيوعًا في كبار السن الفئات العمريةمع ما يصاحب ذلك من داء السكري من النوع 2 - من 0.5 إلى 20٪.
تغييرات تخطيط القلب في MI
يعد تخطيط القلب الكهربائي القياسي (12 خيوطًا) أحد الطرق الرئيسية لتوضيح تشخيص احتشاء عضلة القلب ، وتوطينه ومدى الضرر الذي يصيب عضلة القلب ، ووجود المضاعفات - طبيعة عدم انتظام ضربات القلب والتوصيل.
العلامات المميزة لـ MI أثناء تسجيل ECG هي وجود موجة مرضية Q (العرض - 0.04 ثانية ، العمق يتجاوز 25 ٪ من سعة الموجة R) ، انخفاض في جهد الموجة R - منطقة نخر ؛ إزاحة الجزء ST أعلى أو أسفل العزل بمقدار 2 سم (ارتفاع المقطع ST - طبقة تحت القلبية ، انخفاض في المقطع ST - طبقة تحت الشغاف) - منطقة الضرر الإقفاري ؛ ظهور موجات T "التاجية" الذروة ، الموجبة أو السلبية - نقص التروية (الشكل 1).
أرز. 1.
حاليًا ، في الممارسة السريرية ، اعتمادًا على وجود أو عدم وجود موجة Q مرضية على مخطط كهربية القلب ، احتشاء عضلة القلب "Q-تشكل" (كبير البؤرة أو عبر الجافية) و "Q-non-تشكل" (تحت الشغاف ، تحت القلب ، داخل العضلة) يتميزون. تتوافق تغييرات تخطيط كهربية القلب المماثلة مع وجود لويحة تصلب الشرايين غير المستقرة وتطور خثرة على سطح اللويحة المصابة مع انسداد جزئي أو كامل للشريان التاجي. (الصورة 2).

أرز. 2.ديناميات اللويحات غير المستقرة مع تكوين جلطة وتغيرات مميزة في مخطط كهربية القلب.
بالنسبة لـ MI "تشكيل Q" ، يتم تسجيل التغييرات المميزة على مخطط كهربية القلب:
- ظهور Q- الأسنان المرضية أو مجمع QS (نخر عضلة القلب) ؛
- تقليل سعة الموجة R ؛
- ارتفاع (ارتفاع) أو انخفاض (انخفاض) مقاطع ST من المنطقة المقابلة (طبقات تحت القلب أو تحت الشغاف ، على التوالي) من الضرر الإقفاري ؛
- ربما ظهور حصار على الساق اليسرى لحزمة له.
بالنسبة إلى IM "غير المكون لـ Q" ، التغييرات التاليةعلى مخطط كهربية القلب:
- تحول مقاطع ST من العزل: الارتفاع - طبقة تحت القلب ، انخفاض - طبقة تحت الشغاف ؛
- تقليل سعة الموجة R ؛
- انعكاس ثنائي الطور أو الموجة T ؛
- لا Q- الموجة.
مما لا شك فيه أن إمكانية المقارنة مع مخطط كهربية القلب الذي يسبق فترة ما قبل الاحتشاء والمراقبة اليومية لها أهمية كبيرة في تشخيص احتشاء القلب ECG.
من وجهة نظر عملية ، الأكثر علامات مبكرةتطور MI هو إزاحة الجزء ST من العزلة بمقدار 2 سم أو أكثر ، والتي عادة ما تسبق ظهور موجة Q ، ويمكن تسجيلها بعد 15-20 دقيقة من ظهور متلازمة الألم.
بالنسبة إلى MI ، تعد ديناميكيات تغييرات مخطط كهربية القلب مميزة ، اعتمادًا على توقيت تطورها ومراحل عمليات الإصلاح في منطقة النخر.
يتم تسجيل تحولات المقاطع ST على مخطط كهربية القلب في الساعات الأولى من المرض ، ويمكن أن تستمر لمدة تصل إلى 3-5 أيام ، تليها العودة إلى العزل وتشكيل موجة T سلبية أو ثنائية الطور. MI ، يمكن أن يستمر تحول مقطع ST لعدة أسابيع.
قد يعكس الارتفاع المطول للجزء ST مع موجة QS ("مخطط كهربية القلب المجمد") التهاب التامور الغضروفي من احتشاء عضلة القلب عبر العصب ، ومع التواجد المتزامن لـ R aVR (أعراض Goldberger) هو علامة على تمدد الأوعية الدموية في القلب.
بعد 3-4 ساعات من بداية النوبة الإقفارية ، يتم تسجيل موجة Q (نخر عضلة القلب) على مخطط كهربية القلب في الخيوط مع مقطع ST متحرك. في الوقت نفسه ، يتم تسجيل انخفاض متبادل (متعارض) في مقطع ST في خيوط معاكسة ، مما يشير إلى شدة العملية المرضية.
موجة Q - علامة مستمرة على نخر عضلة القلب أو ندبة ما بعد الاحتشاءومع ذلك ، في بعض الحالات ، قد ينخفض أو يختفي (بعد بضع سنوات) - في حالات تضخم تعويضي لألياف عضلة القلب المحيطة بمركز النخر أو الندبة.
يتميز MI بتكوين موجة T عميقة ، سلبية ، متناظرة ("الشريان التاجي") في 3-5 أيام من المرض في مخطط كهربية القلب يؤدي إلى موقع تلف عضلة القلب الإقفاري ، مع عودة موازية إلى عزل الجزء ST. يمكن أن تستمر الموجة T السلبية المتكونة لعدة أشهر ، لكنها تصبح إيجابية بعد ذلك في معظم المرضى ، مما يشير إلى علامتها التشخيصية على نقص التروية ، وليس الضرر.
للتشخيص الموضعي لـ MI ، من المفيد تسجيل مخطط كهربية القلب في 12 خيوطًا قياسية: الأول والثاني والثالث و aVR و aVL و aVF و V 1-6. دائمًا تقريبًا ، تشارك المناطق المجاورة من البطين الأيسر في العملية النخرية أثناء نقص تروية عضلة القلب ؛ لذلك ، لوحظت تغييرات تخطيط القلب في خصائص MI في العديد من الخيوط المقابلة لمناطق مختلفة من القلب.
الأمامي MI- تغييرات في أنا ، aVL ، ف 1-3يؤدي ECG.
أدنى (حجابي) MI- تغييرات في الثالث ، aVFيؤدي ECG.
قمي الوحشي MI- تغييرات في الثاني ، aVL ، V 4-6يؤدي ECG.
الحاجز الأمامي MI- تغييرات في أنا ، aVL ، ف 1-4يؤدي ECG.
MI السفلي الجانبي- تغييرات في II ، III ، aVL ، aVF ، V 5.6يؤدي ECG.
أمامي الحاجز قمي- تغييرات في أنا ، aVL ، ف 1-4يؤدي ECG.
الخلفي MI- مظهر السن ص ، صالخامس V 1-2، تحول المنطقة الانتقالية من الإصدار 3.4الخامس الإصدار 2.3، متبادل انخفاض مقطع STالخامس الخامس 1-3 يؤدي.
تظهر بعض الصعوبات التشخيصية في 12 مؤشرًا قياسيًا لتخطيط القلب في احتشاء عضلة القلب الخلفي القاعدي. يتميز هذا التوطين بظهور تغييرات متبادلة فقط: ظهور r ، موجات R في V 1.2 يؤدي ، انخفاض المقطع ST في الخيوط I ، V 1-3 وانخفاض في سعة الموجة R في الخيوط V 5.6 (تين. 3). معلومات إضافيةحول توطين MI الخلفي عن طريق تسجيل الخيوط V7-9 (من الخلف) ، حيث يمكن اكتشاف موجات Q المرضية والديناميات المميزة لشريحة ST وموجة T. الأشخاص الأصحاءيمكن أن تسجل ما يكفي عميق Q- الشق(حتى 1/3 من سعة الموجة R). تعتبر الموجة 0 المرضية في الخيوط V 7-9 مدتها> 0.03 ثانية.

أرز. 3.
تسجيل خيوط إضافية في V 4-6 ضلعان أعلى (2-3 مسافة بين الضلوع على يسار القص) ضروري في حالة الاشتباه في توطين أمامي-جانبي مرتفع لـ MI ، عندما يتم الكشف عن التغييرات في مخطط كهربية القلب القياسي فقط في الرصاص aVL.
وفقًا لطبيعة التغييرات في خيوط تخطيط القلب ، يمكن للمرء أن يحكم بشكل غير مباشر على موقع آفة الشرايين التاجية. (الجدول 1).
الجدول 1. منطقة MI اعتمادا على توطين انسداد الشريان التاجي
|
توطين MI |
انسداد الشريان التاجي |
تغييرات تخطيط القلب |
|
الداني الأمامي |
LCA - فوق فرع الحاجز | |
|
الوسيط الأمامي |
LCA - بين الفروع الحاجزة والقطرية | |
|
القاصي الأمامي |
LKA - تحت فرع قطري كبير | |
|
الداني الأدنى |
مغلف LCA أو RCA القريب |
STV5.6 ، II ، III ، aVF |
|
القاصي السفلي |
جهاز كمبيوتر أقل | |
|
القاعدي الخلفي |
الغلاف الخلفي لـ LCA والأقسام السفلية من RCA |
انخفاض متبادل في STV1-3. ص ، R إلى V 1-2 |
|
شغاف دائري |
هزيمة الفروع الصغيرة لـ LCA و RCA |
انخفاض مقطع ST في جميع خيوط ECG |
يحدث النوع الأكثر شدة من احتشاء عضلة القلب عندما يتوقف تدفق الدم في الشريان الأمامي القريب بين البطينين قبل أن يغادر فرع الحاجز الأول. إن توطين الانسداد ووقف تدفق الدم إلى منطقة كبيرة من عضلة القلب له أهمية حاسمة في تقليل النتاج القلبي. مع توطين تلف عضلة القلب الإقفاري ، يتم تسجيل ارتفاعات مقطع ST على مخطط كهربية القلب في جميع الخيوط السابقة - V 1-6 ، في الرصاص القياسي I و aVL. (الشكل 4). توطين الانسداد في الشريان التاجي القريب مصحوبًا بانتهاك إمداد الدم إلى نظام التوصيل للقلب مع انتهاك لتوصيل الإثارة: يتميز تطور شبه الكتلة الأمامية اليسرى ؛ حصار الساق اليسرى أو اليمنى لحزمة له ؛ من الممكن ظهور الحصار الأذيني البطيني بدرجات متفاوتة ، حتى الحصار الكامل للجزء الأوسط من حزقته - حصار موبيتز II (حصار Mobitz I - حصار كامل على المستوى A-Vروابط).

أرز. 4.تضيق حرج للقسم القريب (قبل مغادرة فرع الحاجز) للشريان التاجي الأمامي بين البطينين مع تكوين الحاجز الأمامي MI مع انتشاره إلى القمة والجدار الجانبي للبطين الأيسر.
وقف تدفق الدم في الشريان بين البطينين القريب أسفل منشأ فرع الحاجز الأول مصحوبًا بتطور احتشاء عضلة القلب في القسم الأمامي الأوسط من جدار البطين الأيسر ، مع تسجيل ارتفاع المقطع ST في V 3. 5 وأنا معيارية الرصاص ، دون اضطرابات في توصيل الإثارة في نظام التوصيل للقلب. (الشكل 5). غالبًا ما يكون احتشاء عضلة القلب الأمامي مصحوبًا بنوع ديناميكي مفرط من ديناميكا الدم - عدم انتظام دقات القلب مع زيادة في ضغط الدم (زيادة انعكاسية في أعراض التوتر).

أرز. 5.تضيق حرج في الشريان التاجي النازل الأمامي القريب مع تكوين احتشاء عضلي أمامي - الحاجز - قمي
مع انسداد الشريان الأمامي بين البطينين أسفل مكان منشأ الفرع المائل ، يتم تشكيل MI الأمامي السفلي مع انتشار إلى قمة البطين الأيسر والجدار الجانبي للبطين الأيسر ، والذي يتجلى في تعويض تخطيط القلبالمقطع في I و aVL و V 4-6 خيوط. MI لهذا التوطين لديه صورة سريرية أقل حدة. يمكن أن يشتمل هذا النوع من احتشاء عضلة القلب على متغيرات لها مساحة صغيرة من التلف وينتج عن انسداد أحد الفروع القطرية للشريان التاجي الأيسر ، مما يؤدي إلى تلف الأجزاء الجانبية من البطين الأيسر. في مخطط كهربية القلب مع هذا المتغير ، يتم تسجيل MI عن طريق إزاحة المقطع ST في الخيوط II و aVL و V 5.6 (الشكل 6).

أرز. 6.علامات مخطط كهربية القلب (ECG) للاحتشاء العضلي الجانبي الأمامي مع انتشار إلى الجدار السفلي للبطين الأيسر
يمد الشريان التاجي الأيمن الدم إلى الجدران الجانبية الخلفية السفلية للبطين الأيمن وجدار الحاجز الخلفي للبطين الأيسر. انسداد المحيط الأيمن و / أو الخلفي للشرايين التاجية اليسرى مصحوب بآفات في المناطق المذكورة أعلاه ، غالبًا مع تطور احتشاء عضلي في البطين الأيمن. على مخطط كهربية القلب ، يتم تسجيل ظهور موجات r ، R في V 1-3 مع انخفاض متبادل في مقاطع ST في نفس الخيوط ، مع تحول في منطقة الانتقال من V 3.4 إلى V 1.2. (الشكل 7). سيشير وجود موجة Q مرضية في خيوط إضافية VR 1-3 (متناظرة مع خيوط الصدر اليسرى) إلى حدوث تلف في عضلة القلب في البطين الأيمن. غالبًا ما يكون MI الخلفي معقدًا بسبب تطور درجات متفاوتة من الكتلة الأذينية البطينية.

أرز. 7.تضيق حرج للشريان التاجي الأيمن في منطقة منشأ فرع الحافة المنفرجة ، مع تكوين MI الخلفي السفلي: على مخطط كهربية القلب - QSh ، aVF ، ارتفاع الجزء ST الجزء الثالث ، aVF ، انخفاض متبادل في المقطع ST في الخيوط V1 ، 2 ، مع إزاحة المنطقة الانتقالية في V2.
عادة ما يصاحب احتشاء عضلة القلب الخلفي السفلي تطور توتر المبهم ، والذي يتجلى في بطء القلب وانخفاض ضغط الدم (نوع من ديناميكا الدم الخافض للضغط) ، والذي يمكن التخلص منه عن طريق إعطاء 0.5 مل من الأتروبين في الوريد.
وبالتالي ، فإن تسجيل ECG (خاصة في الديناميات) يجعل من الممكن تشخيص MI ، وتوطينه ، وتحديد طبيعة ومستوى حدوث اضطرابات التوصيل ، وإيقاع القلب ، مما يعقد مسار علم الأمراض.
يجب أن نتذكر أن التغييرات المذكورة أعلاه على مخطط كهربية القلب يمكن أن تحدث أيضًا مع أمراض أخرى: التهاب التامور الحاد ، والتهاب عضلة القلب ، والقلب الرئوي الحاد (PE الهائل) ، ومتلازمة عودة الاستقطاب المبكر ، وتضخم عضلة القلب البطيني الأيسر ، والسكتة الدماغية الدماغية الإقفارية أو النزفية ، والكهارل و اضطرابات الغدد الصماءإلخ. غالبًا ما يتم تسجيل التغييرات الشبيهة بالاحتشاء في الموجة Q أو مركب QRS غير الطبيعي على مخطط كهربية القلب في المتلازمات الإثارة المبكرةالبطينين (WPW ، CLC) ، مع تشريح تمدد الأوعية الدموية في الأبهر الصاعد ، والالتهاب الرئوي المزمن والربو القصبي ، والتسمم الحاد من أصول مختلفة.
التشخيص الأنزيمي لاحتشاء عضلات القلب
وفقًا لتوصيات منظمة الصحة العالمية ، في تشخيص AMI ، جنبًا إلى جنب مع العلامات السريرية وتغييرات تخطيط القلب ، تعتبر دراسات العلامات الخاصة بالقلب ذات أهمية كبيرة. حاليًا ، هناك عدد كافٍ من علامات موت خلايا عضلة القلب معروفة ، والتي لها درجة مختلفة من الخصوصية لعضلة القلب ، مما يسمح لنا بتقييم حجم وتوقيت تطور النخر وطبيعة مسار المرض.
تزداد القيمة التشخيصية للتشخيص المختبري لاحتشاء عضلة القلب بشكل كبير مع الأشكال غير المؤلمة ومع احتشاء عضلة القلب المتكرر والرجفان الأذيني ووجود جهاز تنظيم ضربات القلب الاصطناعي المزروع (EC) ، أي. في الحالات التي يكون فيها تشخيص احتشاء عضلة القلب ECG صعبًا.
حاليًا ، في الممارسة السريرية ، غالبًا ما يتم استخدام تركيزات العلامات المحددة التالية لتلف عضلة القلب: ميوغلوبين (Mg) ، كارديوتروبونين (TnI ، TnT) ، فوسفوكيناز الكرياتين (CPK) ، أسبارتات أمينوترانسفيراز (ACT) ، نازعة هيدروجين اللاكتات (LDH) ، فسفوريلاز الجليكوجين (GP). (الشكل 8).

أرز. 8.ديناميات الإنزيمات الخاصة بالقلب في MI غير المعقد.
الميوغلوبين ، الإنزيمات المتساوية - جزء CPK-MB ، الكارديوتروبونين - TnI ، الجليكوجين فسفوريلاز - GF-BB خاصة بهزيمة خلايا عضلة القلب فقط (ولكن ليس الخلايا العضلية الهيكلية العضلية).
منذ التسعينيات من القرن العشرين ، ظهرت إمكانيات تقنية لتحديد والاستخدام السريري في تشخيص MI لاثنين من البروتينات الهيكلية داخل الخلايا لخلايا عضلة القلب ، مما يشير إلى موت عضلة القلب - ميوغلوبين إيتروبونين.
الميوغلوبين هو الأقدم والأكثر حساسية للضرر الذي يصيب خلايا عضلة القلب. المغنيسيوم هو بروتين هيكلي للخلية العضلية ، مع تلف عضلة القلب يتم تحديده في مصل الدم عن طريق المقايسة المناعية الإشعاعية. يتميز اختبار الميوغلوبين بحساسية وخصوصية عاليتين ، مما يتجاوز معايير إنزيمات الإنزيمات الخلوية الخاصة بعضلة القلب. تبدأ الزيادة في تركيز المغنيسيوم في مصل الدم بعد 1-3 ساعات من ظهور متلازمة الألم ، وتصل إلى حد أقصى قدره 6-7 ساعات من المرض ، ومع مسار غير معقد من MI ، تعود إلى طبيعتها من قبل نهاية اليوم الأول من العملية المرضية.
البروتين الهيكلي الثاني لخلايا عضلة القلب - تروبونين ، الذي يشارك في تنظيم وظيفة الخلية العضلية - الانكماش والاسترخاء ، هو جزء من مركب تروبوميوسين-تروبونين ، ويتكون من ثلاثة ببتيدات (TnC و TnI و TnT). يحتوي TnT على 3 أشكال إسوية: 2 عضلي هيكلي - TnT 2،3 و 1 عضلة القلب - TnT 1. يكون TnI القلبي موضعيًا فقط في عضلة القلب ويتم إطلاقه أثناء نخر خلايا عضلة القلب. يستخدم Cardiac Troponin TnT أيضًا كعلامة على نخر عضلة القلب ، ولكن يمكن أن يزيد محتواه أيضًا مع زيادة العضلات الهيكلية. تبدأ تركيزات TnT و TnI في الزيادة المستويات العاديةبعد 5-12 ساعة من بداية نقص التروية ، تصل الذروة بنهاية اليوم الأول (بعد 24 ساعة) - TnI وبنهاية اليوم الثاني (48 ساعة) - تطور TnT of MI. ينتهي تطبيع هذه العلامات الخاصة بالقلب في غضون 5-10 أيام.
التشخيص الأنزيمي لاحتشاء عضلة القلب ليس فقط طريقة تكمل العلامات السريرية ، ولكن أيضًا معيار مستقل عند اتخاذ قرار بشأن علاج التخثر ، إعادة توعية عضلة القلب الغازية في الساعات الأولى من تطور الانسداد عن طريق تجلط الشرايين في الشريان التاجي في الأشكال السلبية لتخطيط كهربية القلب. MI.
في الممارسة السريرية ، في تشخيص MI ، يتم استخدام تحديد تركيز المصل من إنزيم فوسفوكيناز الكرياتين الخلوي الخاص بالأعضاء - CPK على نطاق واسع. في البشر ، يتكون CPK من وحدتين فرعيتين (M و B) ، والتي تشكل 3 أشكال من الإنزيمات المتشابهة: MM - نوع العضلات، BB - نوع الدماغ ، MB - نوع القلب ( إجمالي CPK = S CPK-MB + CPK-MM + CPK-BB). يبدأ نشاط جزء CK MB في احتشاء عضلة القلب في الزيادة بعد 6 ساعات ، ويصل إلى الحد الأقصى بعد 24 ساعة من بداية المرض ويعود إلى طبيعته بنهاية اليوم الثاني من MI. التشخيص زيادة كبيرةنشاط جزء CPK MB يزيد بمقدار ضعف ونصف عن المعيار المعتمد في هذا المختبر. تقليديا ، يوصى بتحديد نشاط إنزيم CPK كل 6-8 ساعات من أجل تحديد حجم تلف عضلة القلب (منطقة منحنى نشاط الإنزيم المتماثل) وطبيعة مسار المرض (معقد وغير معقد) ).
يتم توزيع إنزيمات aminotransferases (aspartate amino- و alanine aminotransferases) بشكل عام داخل الخلايا (السيتوبلازمية والميتوكوندريا) ، والتي يستخدم تحديد نشاطها تقليديا في الممارسة السريرية لتشخيص MI. بعد أن بدأ نشاطهم في الزيادة بنهاية اليوم الأول للمرض ، يصل إلى الحد الأقصى بنهاية اليوم الثاني ويعود إلى طبيعته بنهاية اليوم الثالث من بداية MI. محدد لهزيمة عضلة القلب هو زيادة نسبة ACT إلى ALT بمقدار 2.5 مرة (مؤشر De Rites). مع التنفيذ النشط والاستخدام على نطاق واسع في الممارسة السريريةتشخيص MI ، تحديد نشاط إنزيمات CPK و Tn الخاصة بالأعضاء ، يظل الدافع الرئيسي لتحديد AST / ALT هو رخص هذه الدراسات وتوافرها.
إنزيم آخر خاص بعضلة القلب يستخدم في تشخيص متلازمة AMI ومتلازمات الشريان التاجي هو إنزيم اللاكتات ديهيدروجينيز (LDH) ، والذي يتكون من 5 إنزيمات متوازنة تحتوي على نوعين من سلاسل عديد الببتيد (M و H). يحتوي الإنزيم المتماثل الموجود في الغالب في عضلة القلب على 4 سلاسل H متطابقة ويتم تحديده على أنه LDH1 ، ويتم تصنيف نظير الإنزيم الذي يحتوي على 4 سلاسل M متطابقة على أنه LDH5. يبدأ نشاط إنزيمات LDH الخاصة بعضلة القلب في الزيادة من نهاية اليوم الأول للمرض ، ويصل إلى الحد الأقصى بحلول اليوم الثالث ويعود إلى طبيعته بحلول اليوم الخامس والسادس من تطور MI. يجب تحديد نشاط LDH يوميًا لمدة ثلاثة أيام.
تعتمد القيمة التشخيصية للعلامات الموضحة أعلاه لتلف خلايا عضلة القلب على توقيت وتكرار تحديدها في ديناميكيات AMI. Paognomonic for MI هو زيادة في نشاط الإنزيم بما لا يقل عن 1.5-2 مرات من المستوى الطبيعي ، يليه انخفاض إلى القيم الطبيعية.
لذلك ، فإن الاستخدام الفردي لواسمات عضلة القلب في المرضى الذين يشتبه في إصابتهم بالـ AMI أمر غير مقبول ويقلل تمامًا تقريبًا من الأهمية التشخيصية لهذه التقنيات.
البحوث السريرية والمخبرية
في العديد من المرضى الذين يخضعون لاحتشاء عضلة القلب ، هناك زيادة في درجة الحرارة - حالة فرط الحمية ، والتي تترافق مع زيادة عدد الكريات البيضاء العدلات حتى 12-14109 / لتر بدون طعنة التحول المميزة للالتهاب الرئوي. يترافق كثرة الكريات البيضاء العدلات في MI مع فرط الحمضات المعتدل. مع انخفاض عدد الكريات البيضاء (في اليوم الثالث والرابع من بداية المرض) ، يتم تحديد ESR المتسارع في الدم المحيطي (أحد أعراض "المقص") ، والذي يظل مرتفعًا لمدة أسبوع إلى أسبوعين.
يتميز MI بزيادة مستويات الفيبرينوجين و رد فعل إيجابيبروتين سي التفاعلي.
عند فحص مخطط تجلط الدم في الفترة الحادة من MI ، يتم تسجيل ميل إلى فرط التخثر مع ظهور منتجات تحلل الفيبرينوجين (FDP) وزيادة تركيز D-dimer (أحد أجزاء سلسلة الفبرين في الدم الجلطة) ، مما يشير إلى التنشيط التلقائي لنظام التحلل الفبري استجابة لتشكيل الجلطة.
دراسات تخطيط صدى القلب في احتشاء عضلة القلب الحاد
منذ عام 1954 ، عندما تم تقديم التقارير الأولى عن استخدام تقنية الموجات فوق الصوتية في التشخيص بواسطة Edler و Hertz آفات الصماماتو عيوب خلقيةمن القلب ، خضع تخطيط صدى القلب لتغييرات كبيرة من اكتساح الوقت (الوضع M) إلى الموجات فوق الصوتية ثنائية وثلاثية الأبعاد الهياكل التشريحيةوغرف القلب في الوقت الحقيقي.
يسمح لك المسح بالموجات فوق الصوتية القطاعي ثنائي الأبعاد بإجراء تقييم ديناميكي لأبعاد الغرف ، وسماكة وحركة جدران القلب ، بالإضافة إلى انتهاكات وظائف الإغلاق لجهاز الصمامات والهياكل التشريحية داخل القلب. يعطي وجود مناطق نقص الحركة ، والحركة ، وخلل الحركة فكرة عن توطين وحجم احتشاء عضلة القلب ، وتوفر المراقبة الديناميكية لتقلص هذه المناطق معلومات قيمة حول تطور العملية المرضية. يعطي تقييم ديناميكا الدم داخل القلب (جزء القذف القلبي) فكرة عن حجم الآفة وضعف وظيفة ضخ القلب.
يعد تخطيط صدى القلب على النقيض من إحدى الطرق الواعدة لتشخيص صلاحية عضلة القلب. عندما تدار عن طريق الوريد عامل تباين(الفسفوليبيدات أو الألبومين بأحجام من 2.5 إلى 5 ميكرون) يزداد تباين صدى الدم في تجاويف القلب وسرير الأوعية الدموية الدقيقة لعضلة القلب بما يتناسب مع حجم تدفق الدم. تتيح أجهزة الموجات فوق الصوتية الحديثة المزودة بتقنيات جديدة إمكانية تدمير الهياكل الدقيقة لعامل التباين في تجاويف القلب بسرعة ، وبناءً على معدل إعادة التراكم والغسيل اللاحق ، قم بحساب القيمة المطلقة لتروية عضلة القلب (بالمللي / g / min) ، والذي لا يسمح فقط بتحديد مناطق التندب وعضلة القلب القابلة للحياة. هذه الطريقة تجعل من الممكن تقييم درجة "ذهول" عضلة القلب وتحديد مناطق عضلة القلب السبات.
يكشف تخطيط صدى القلب بالإجهاد الدوائي (تخطيط صدى القلب بالإجهاد) باستخدام الدوبوتامين (5-10 ميكروغرام / كغ / دقيقة) عن "السبات" عضلة القلب ودرجة "الذهول".
وبالتالي ، باستخدام تخطيط صدى القلب ، من الممكن تشخيص منطقة الضرر ودرجة انتهاك وظيفة ضخ القلب في الديناميات ، والتي على أساسها يتم تقييم فعالية العلاج والتنبؤ بالتطور من المرض.
ومع ذلك ، فإن هذه الطريقة لها إمكانيات محدودة في حالات السمات التشريحية للصدر (ضيق المساحة الوربية ، وانتهاكات العلاقات التشريحية للأعضاء المنصفية) وتغيرات انتفاخ الرئة في أنسجة الرئة التي تمنع انتشار حزمة المسح بالموجات فوق الصوتية.
تشخيص متباين
في بعض الحالات ، يجب التمييز بين احتشاء عضلة القلب الحاد وأمراض أخرى ، حيث يمكن أن يكون الألم الشديد في الصدر ناتجًا عن عدة أمراض. العمليات المرضيةفي أعضاء الصدر وتجويف البطن وأنظمة أخرى في جسم الإنسان.
1. أمراض الجهاز القلبي الوعائي:
- عضلة القلب الضخامي؛
- التهاب التامور الحاد.
- التهاب عضلة القلب الحاد
- الانسداد الرئوي؛
- تشريح تمدد الأوعية الدموية الأبهري.
2. أمراض الرئة وغشاء الجنب:
- الالتهاب الرئوي الحاد
- استرواح الصدر العفوي.
3. أمراض المريء والجهاز الهضمي:
- التهاب المريء.
- رتج المريء:
- فتق في فتحة المريء من الحجاب الحاجز.
- قرحة المعدة؛
- التهاب المرارة والبنكرياس الحاد.
4. أمراض الجهاز الحركي:
- الداء العظمي الغضروفي في العمود الفقري العنقي.
- التهاب الضفيرة الكتف.
- التهاب العضل.
- الألم العصبي الوربي (القوباء المنطقية).
وبالتالي ، فإن المعايير الرئيسية للتشخيص التفريقي لاحتشاء عضلة القلب هي:
أ - وجود نوبة ألم ذبحة صدرية نموذجية أو وجود إزعاج في الصدر ؛
ب - التغييرات المميزة في تخطيط القلب ؛
ب - زيادة في العلامات القلبية النوعية لنخر عضلة القلب. من الضروري المراقبة الديناميكية للمحددات المذكورة أعلاه لتقييم فعالية العلاج والوقاية. المضاعفات المحتملة، لتنظيم تكتيكات فترة إعادة التأهيل والتنبؤ بحياة المرضى الذين خضعوا لاحتشاء عضلة القلب.
احتشاء عضلة القلب. أكون. شيلوف
تشخيص احتشاء عضلة القلبقائم على
في متلازمة الألم الإقفاري التقليدية (أو انزعاج الصدر) ،
التغييرات النموذجية في تخطيط القلب أثناء التسجيل الديناميكي (في نصف المرضى الذين تم إدخالهم إلى المستشفى مع وجود ألم في القلب واشتباه في احتشاء عضلة القلب ، تم الكشف عن مخطط كهربية القلب غير المشخص) ،
تغييرات كبيرة (زيادة ثم التطبيع) في مستويات الإنزيمات الخاصة بالقلب في مصل الدم ،
مؤشرات غير محددة لنخر الأنسجة والالتهاب (متلازمة الارتشاف) ،
EchoCG وبيانات التصوير الومضاني للقلب
معظم حالات احتشاء عضلة القلبتم وضعه بالفعل على أساس الصورة السريرية ، حتى قبل أخذ مخطط كهربية القلب ، يسمح مخطط كهربية القلب بتشخيص احتشاء عضلة القلب في 80٪ من الحالات ، ولكنه لا يزال أكثر ملاءمة لتوضيح توطين ووصف احتشاء عضلة القلب أكثر من تحديد حجم بؤرة النخر (يعتمد الكثير على وقت أخذ مخطط كهربية القلب) غالبًا ما يكون هناك ظهور متأخر للتغيرات في مخطط كهربية القلب. وبالتالي ، في الفترة المبكرة من احتشاء عضلة القلب (الساعات الأولى) ، قد تكون معلمات تخطيط القلب طبيعية أو صعبة يفسر.
حتى مع وجود احتشاء واضح لعضلة القلب ، قد لا يكون هناك زيادة في الفاصل الزمني ST وتشكيل موجة مرضية Q. لذلك ، من الضروري تحليل تخطيط القلب في الديناميكيات. تسجيل تخطيط القلب في الديناميات خلال الفترة ألم إقفاريسيساعد في تقييم تطور التغييرات في معظم المرضى. لذلك ، يجب على كل مريض يعاني من ألم في الصدر يحتمل أن يكون مصابًا بالقلب أن يسجل مخطط كهربية القلب في غضون 5 دقائق ويقيمه على الفور من أجل تحديد مؤشرات لعلاج إعادة التروية إذا أظهر مخطط كهربية القلب ارتفاعًا "جديدًا" في مقطع ST أو حصار LDL "جديد" ، هذا مؤشر على ضخه بشكل كافٍ مع تحلل الخثرة الجهازي أو PTCA
معايير احتشاء عضلة القلب "الجديد"- الزيادة النموذجية والنقص التدريجي في العلامات البيوكيميائية لنخر عضلة القلب (اختبار تروبونين) أو زيادة ونقصان أسرع في CK-MB بالاقتران مع واحدة على الأقل من الأعراض التالية لنقص التروية ، ظهور موجة Q غير طبيعية على مخطط كهربية القلب ، تغيرات تخطيط القلب تشير إلى نقص التروية (زيادة أو نقصان مميزان في الفترة ST) ، والتدخل التاجي (رأب الوعاء) ، والعلامات التشريحية والمرضية لاحتشاء عضلة القلب "الجديد".
تظهر التجربة أن النصف تقريبا مرضى احتشاء عضلة القلبوجود بداية غير مؤلمة للمرض (أو مظهر غير نمطي لمتلازمة الألم) ولا توجد تغيرات واضحة (مفسرة بشكل لا لبس فيه) في مخطط كهربية القلب
المعايير الرائدة لتخطيط القلب لاحتشاء عضلة القلب.
1) انعكاس الموجة T ، مما يشير إلى نقص تروية عضلة القلب غالبًا ما يفوت الطبيب هذه التغييرات الحادة ،
2) في الفترة الحادة ، تتشكل موجة T عالية الذروة (نقص التروية) ويمكن أن تندمج الزيادة في الجزء ST (الضرر) ، الذي له شكل محدب (أو صاعد بشكل غير مباشر) ، مع الموجة T ، مكونة أحادي الطور منحنى (يشير إلى تلف عضلة القلب) قد يكون التغيير في الجزء الأخير من المجمع البطيني (ارتفاع أو انخفاض الفاصل الزمني ST وانقلاب الموجة T اللاحقة) مظاهرًا لاحتشاء عضلة القلب صغير البؤرة (احتشاء عضلة القلب بدون Q).
للموافقة على تشخيص احتشاء عضلة القلب بدون Q ، من الضروري زيادة الإنزيمات (يفضل أن تكون خاصة بالقلب) بما لا يقل عن 1.5-2 مرات.بدون ذلك ، يظل تشخيص احتشاء عضلة القلب افتراضياً ،
3) ارتفاع الفاصل الزمني ST بمقدار 2 مم أو أكثر في اثنين على الأقل من الخيوط المتجاورة (غالبًا ما يقترن بانخفاض "مرآة" في الفاصل الزمني ST في الخيوط من الجدار المقابل للقلب) ،
4) تطور موجة Q المرضية (أكثر من 1/4 من السعة R في الخيوط V1-6 و avL ، أكثر من 1/2 من السعة R في الخيوط II و III و avF ، فاصل QS في V2- 3 على خلفية سلبية T ، Q أكثر 4 مم في V4-5). يشير إلى موت خلايا عضلة القلب إن ظهور موجة مرضية Q (تحدث بعد 8-12 ساعة من ظهور الأعراض ، ولكن قد تكون لاحقًا) هو نموذجي للـ MI كبير البؤرة (مع موجات Q و R) و transural (QS) في كثير من الأحيان في المرضى الذين يعانون من Q والارتفاع الفاصل ST في منطقة واحدة يتم تحديده من خلال انخفاض في الفاصل الزمني ST في مناطق أخرى (غير احتشاء) (نقص التروية على مسافة ، أو ظاهرة كهربائية متبادلة).
معايير تخطيط القلب لتشخيص احتشاء عضلة القلبمع زيادة في الفاصل الزمني ST - وجود ألم في الصدر وأي من العلامات التالية على الخلفية:
موجة Q مرضية جديدة أو مشتبه بها في خيوط 2 على الأقل من التالي: II ، III ، V1-V6 أو I و avL ؛
ارتفاع أو انخفاض فاصل ST-T جديد أو مشتبه به ؛
حصار كامل جديد للساق اليسرى من صرة صاحب.
احتشاء عضلة القلب(يحدث غالبًا على خلفية انخفاض احتشاء عضلة القلب) يتم تشخيصه بشكل سيء في مخطط كهربية القلب التقليدي ، لذلك يلزم رسم خرائط تخطيط القلب أو تسجيل مخطط كهربية القلب في الخيوط اليمنى للصدر (V3r-V4r) ، وزيادة المقطع ST لأكثر من 1 مم في V1 (أحيانًا في V2-3) يؤخذ في الاعتبار أيضًا. في الأيام الأولى من MI ، من الضروري إجراء مخطط كهربية القلب Hm. في الأيام التالية من الفترة الحادة ، يتم تسجيل مخطط كهربية القلب يوميًا.
مع احتشاء عضلة القلب البؤري الصغيرمن الصعب تحديد فتراته على مخطط كهربية القلب عمليًا.
معايير التشخيص لاحتشاء عضلة القلب
يقرأ:
زيادة و (أو) انخفاض لاحق في مستوى العلامات البيوكيميائية لنخر عضلة القلب في الدم (يفضل التروبونين القلبي) ، إذا تجاوز تركيزها في عينة دم واحدة على الأقل الحد الاعلىالمعايير المختبرية وواحد على الأقل من الأدلة التالية على إقفار عضلة القلب:
الصورة السريرية لإقفار عضلة القلب.
تغييرات تخطيط القلب تشير إلى ظهور نقص تروية عضلة القلب (حدوث تشريد للجزء ST-T ،حصار الساق اليسرى لحزمة له) ؛
ظهور الأسنان المرضية سعلى تخطيط القلب.
ظهور علامات فقدان عضلة القلب القابلة للحياة أو ضعف الانقباض الموضعي عند استخدام التقنيات التي تسمح برؤية القلب.
صياغة تشخيص سريري مفصل لـ MIيجب أن تعكس:
طبيعة الدورة (ابتدائي ، متكرر ، متكرر) ؛
عمق النخر (MI مع سن سأو MI بدون أسنان س) ؛
توطين MI ؛
تاريخ حدوث MI ؛
المضاعفات (إن وجدت): اضطرابات النظم والتوصيل ، قصور القلب الحاد ، إلخ ؛
أمراض الخلفية هي تصلب الشرايين التاجية (إذا تم إجراء تصوير الأوعية التاجية ، يشار إلى شدتها وانتشارها وتوطينها) ، ارتفاع ضغط الدم (إن وجد) ومرحلته ، داء السكري ، إلخ.
تتكون مساعدة مرضى احتشاء عضلة القلب الناجم عن ارتفاع مقطع ST من نظام من الإجراءات التنظيمية والعلاجية.
تشمل الأنشطة التنظيمية:
- التشخيص المبكر من قبل أطباء الطوارئ وأطباء المناطق والمعالجين والممارسين العامين للعيادات الشاملة في المنطقة من ACS-ST بناءً على المعايير المقدمة سابقًا (انظر ACS-ST) ؛
- الاستشفاء في أقرب وقت ممكن من قبل فريق الإسعاف لمريض مصاب بـ ST-ACS في وحدة أمراض القلب المكثفة في قسم أمراض القلب في حالات الطوارئ ؛
- في أقرب وقت ممكن ، بدء الإجراءات التي تهدف إلى استعادة تدفق الدم التاجي: إجراء PCI الأولي في غضون 90 دقيقة من لحظة دخول المريض إلى المستشفى مع هذه المرافق ، أو إدخال الأدوية الحالة للخثرة في مرحلة ما قبل دخول المستشفى أو في موعد لا يتجاوز 30 دقيقة من لحظة دخول المريض إلى المستشفى وليس لديه القدرة على إجراء PCI الأولي ؛
- إقامة المريض خلال الفترة الحادة من احتشاء عضلة القلب الناجم عن ارتفاع مقطع ST في وحدة أمراض القلب المركزة ؛
- نظام العلاج التأهيلي (إعادة التأهيل).
يتم تنفيذ التدابير العلاجية مع مراعاة مرحلة احتشاء عضلة القلب الناجم عن ارتفاع مقطع ST وشدة وطبيعة المضاعفات.
في الفترة الأولى من احتشاء عضلة القلب الناجم عن احتشاء عضلة القلب ، تهدف التدابير العلاجية الرئيسية إلى تخفيف الآلام ، والاستعادة الكاملة والمستقرة لتدفق الدم التاجي في الشريان المرتبط بالاحتشاء ، وعلاج المضاعفات ، إن وجدت.
تخفيف الآلام.التخدير من أهم المهام فترة أوليةعلاج مرضى احتشاء عضلة القلب الناجم عن ارتفاع مقطع ST. مع عدم فعالية تناول 0.4 ملغ من النتروجليسرين بمقدار 1-2 ضعفًا على شكل أقراص أو رذاذ ، يتم استخدام المسكنات المخدرة في الوريد ، والتي من بينها محلول 1 ٪ من المورفين (هيدروكلوريد المورفين) هو الأكثر فعالية. عادة ، يتم حقن 1.0 مل من الدواء ، المخفف في 20.0 مل من محلول كلوريد الصوديوم متساوي التوتر ، عن طريق الوريد (ببطء!). بدلاً من المورفين ، يمكن أيضًا استخدام المسكنات المخدرة الأخرى: 1.0 مل من محلول 1٪ من تريبيريدين (بروميدول *) ، 1-2 مل من محلول 0.005٪ من الفنتانيل ، كما هو الحال مع المهدئات أو مضادات الذهان (2 مل من a 0.25٪ محلول دروبيريدول) وكذلك بدونها.
العلاج بالأوكسجينمن خلال قناع الوجه أو القسطرة الأنفية يستخدم للمرضى الذين يعانون من ضيق في التنفس أو علامات سريرية لفشل القلب الحاد (وذمة رئوية ، صدمة قلبية).
استعادة تدفق الدم التاجي ونضح عضلة القلب.إن أسرع استعادة لتدفق الدم في الشريان التاجي المسدود (ضخه) هي مهمة أساسية في علاج المرضى الذين يعانون من احتشاء عضلة القلب الناجم عن ارتفاع مقطع ST ، حيث يؤثر حلها على الوفيات داخل المستشفى والتنبؤ الفوري والطويل الأمد. في الوقت نفسه ، من المستحسن ، بالإضافة إلى أسرع وقت ممكن ، أن تكون استعادة تدفق الدم التاجي كاملة ومستقرة. النقطة الأساسية التي تؤثر على فعالية أي تدخل ضخه ونتائجها على المدى الطويل هي عامل الوقت: فقدان كل 30 دقيقة يزيد من خطر الوفاة في المستشفى بحوالي 1٪.
هناك خياران لاستعادة تدفق الدم التاجي: العلاج التخثر ،أولئك. ضخه مع الأدوية الحالة للخثرة (الستربتوكيناز ، منشطات البلازمينوجين في الأنسجة) ، و PCI ،أولئك. إعادة التروية عن طريق التدمير الميكانيكي للكتل الخثارية التي تسد الشريان التاجي (رأب الوعاء بالبالون وتدعيم الشرايين التاجية).
يجب إجراء محاولة لاستعادة تدفق الدم التاجي بطريقة أو بأخرى في جميع المرضى الذين يعانون من احتشاء عضلة القلب الناجم عن ارتفاع مقطع ST خلال الـ 12 ساعة الأولى من المرض (ما لم تكن هناك موانع). تدخلات ضخ الدم لها ما يبررها أيضًا بعد 12 ساعة من بداية المرض ، إذا كانت هناك علامات إكلينيكية و ECG على نقص تروية عضلة القلب المستمر. في المرضى المستقرين ، في حالة عدم وجود علامات سريرية وعلامات ECG لنقص تروية عضلة القلب المستمر ، لا تتم الإشارة إلى العلاج حال للخثرة أو PCI بعد 12 ساعة من بداية المرض.
حاليًا ، الطريقة المفضلة لاستعادة تدفق الدم التاجي في المرضى الذين يعانون من احتشاء عضلة القلب الناجم عن ارتفاع مقطع ST في أول 12 ساعة من المرض هي التداخل الإكليلي الأولي (الشكل 2-19).

أرز. 2-19.اختيار استراتيجية ضخه لعلاج المرضى الذين يعانون من احتشاء عضلة القلب مع ارتفاع القطعة شارعفي أول 12 ساعة من المرض
تحت PCI الأساسييُقصد بها رأب الوعاء بالبالون مع أو بدون دعامة للشريان التاجي المرتبط بالاحتشاء ، ويتم إجراؤه خلال الـ 12 ساعة الأولى من ظهور الصورة السريرية لمرض احتشاء عضلة القلب الناجم عن احتشاء عضلة القلب الناجم عن احتشاء عضلة القلب الناجم عن احتشاء عضلة القلب الناجم عن احتشاء عضلة القلب بدون استخدام مسبق لمحلل الخثرة أو أدوية أخرى قادرة على إذابة جلطات الدم.
من الناحية المثالية ، في غضون الـ 12 ساعة الأولى من المرض ، يجب نقل مريض احتشاء عضلة القلب إلى مستشفى لديه القدرة على إجراء PCI الأولي على مدار 24 ساعة في اليوم ، 7 أيام في الأسبوع ، بشرط أن يكون التأخير المتوقع بين أول اتصال للمريض بالطبيب وفي اللحظة التي يتم فيها نفخ القسطرة البالونية في الشرايين التاجية (أي لحظة استعادة تدفق الدم التاجي) لن تتجاوز ساعتين. في المرضى الذين يعانون من احتشاء عضلة القلب الشديد الذي تم تشخيصه في أول ساعتين من بداية المرض ، يجب ألا يتجاوز ضياع الوقت 90 دقيقة.
ومع ذلك، في الحياه الحقيقيهبعيدًا عن جميع المرضى الذين يعانون من احتشاء عضلة القلب الناجم عن ارتفاع مقطع ST ، فمن الممكن إجراء PCI الأولي ، لأنه ، من ناحية ، ولأسباب مختلفة ، يتم إدخال أقل من 50٪ من المرضى إلى المستشفى في أول 12 ساعة من المرض ، وأقل من 20٪ من مرضى STEMI. من ناحية أخرى ، ليست كل المستشفيات الكبيرة لديها القدرة على إجراء PCI للطوارئ على مدار 24 ساعة في اليوم ، 7 أيام في الأسبوع.
في هذا الصدد ، في جميع أنحاء العالم ، بما في ذلك الاتحاد الروسي ، لا تزال الطريقة الرئيسية لاستعادة تدفق الدم التاجي لدى مرضى احتشاء عضلة القلب الناجم عن ارتفاع مقطع ST العلاج التخثر.تشمل مزايا العلاج حال التخثر بساطة تنفيذه ، والتكلفة المنخفضة نسبيًا ، وإمكانية تنفيذه في كل من مرحلة ما قبل دخول المستشفى (انخفاض كبير ، على الأقل 30 دقيقة (!) في الوقت قبل بدء العلاج بإعادة ضخ الدم) ، و في اي مستشفى. تشمل عيوبه الفعالية غير الكافية (50-80٪ اعتمادًا على نوع عقار التخثر والوقت المنقضي منذ ظهور المرض) ، والتطور المبكر (5-10٪ من المرضى) والمتأخر (30٪ من المرضى) المتكرر انسداد الشرايين التاجية ، واحتمال حدوث مضاعفات نزفية شديدة ، بما في ذلك السكتة الدماغية النزفية (في 0.4-0.7٪ من المرضى).
في حالة عدم وجود موانع ، يجب إجراء علاج التخثر خلال الـ 12 ساعة الأولى من بداية الصورة السريرية لـ STEMI في المرضى الذين لا يمكن إجراء PCI الأولي لديهم لأي سبب خلال الفترات الزمنية المذكورة أعلاه.
من الأهمية بمكان الموقف الذي يُنصح فيه بتخثر الخثرة الجهازي فقط في أول 12 ساعة من بداية الصورة السريرية لمرض احتشاء عضلة القلب الناجم عن ارتفاع مقطع ST.
في وقت لاحق ، لم تتم الإشارة إلى تجلط الدم الجهازي ، لأن فعاليته منخفضة للغاية ، وليس له تأثير كبير على معدلات الوفيات داخل المستشفى وعلى المدى الطويل.
حاليًا ، أكثر الأدوية المستخدمة على نطاق واسع هي الستربتوكيناز (الدواء الأكثر استخدامًا في العالم) ومنشطات البلازمينوجين في الأنسجة ، والتي تشمل alteplase (t-PA) و reteplase (rt-PA) و tenecteplase (NT-PA) و prourokinase ( بورولاس).
تتمتع منشطات البلازمينوجين النسيجية بميزة لأنها أدوية مسبب للتخثر خاصة بالفيبرين.
في وجود موظفين مدربين ، يوصى ببدء العلاج حال التخثر في مرحلة ما قبل دخول المستشفى في فريق الإسعاف ، والذي يمكن أن يقلل بشكل كبير (بما لا يقل عن 30-60 دقيقة) من ضياع الوقت المرتبط بتدخلات إعادة ضخ الدم.
مؤشرات لانحلال الخثرة الجهازي:
وجود صورة سريرية نموذجية لمتلازمة الشريان التاجي الحادة بالتزامن مع تغيرات تخطيط القلب في شكل ارتفاع القطعة شارع> 1.0 مم في 2 من أطراف التوصيل القياسية للأطراف المتجاورة أو ارتفاع الجزء ST> 2.0 مم في طرفين متجاورين من الصدر أو أكثر ؛
لأول مرة ، تم الكشف عن حصار كامل للفرع الأيسر من حزقته مع صورة سريرية نموذجية.
ل موانع مطلقة
السكتة الدماغية النزفية أو السكتة الدماغية ذات الطبيعة غير المعروفة لأي وصفة طبية في التاريخ ؛
السكتة الدماغية خلال الأشهر الستة الماضية.
وجود أمراض الأوعية الدموية في الدماغ (التشوه الشرياني الوريدي) ؛
التوفر ورم خبيثالدماغ أو النقائل.
الصدمة الحديثة ، بما في ذلك الصدمات الدماغية ، عملية في البطن، خلال الأسابيع الثلاثة الماضية ؛
نزيف الجهاز الهضمي خلال الشهر الماضي ؛
أمراض معروفة مصحوبة بنزيف.
الاشتباه في تشريح جدار الأبهر.
ثقوب الأعضاء غير القابلة للانضغاط (ثقب الكبد ، البزل القطني) ، بما في ذلك الأوعية (الوريد تحت الترقوة).
ل موانع نسبيةيشمل تحلل الخثرة الجهازي:
نوبة نقص تروية عابرة خلال الأشهر الستة الماضية ؛
العلاج بمضادات التخثر غير المباشرة.
الحمل والأسبوع الأول بعد الولادة ؛
إنعاش مصحوب بإصابة في الصدر ؛
ارتفاع ضغط الدم غير المنضبط (ضغط الدم الانقباضي> 180 ملم زئبق) ؛
القرحة الهضمية و الاثنا عشريفي المرحلة الحادة
أمراض الكبد المتقدمة.
يتم إعطاء الستربتوكيناز عن طريق الوريد بجرعة 1.5 وحدة ، مذابة في 100 مل من محلول كلوريد الصوديوم 0.9٪ أو 5٪ جلوكوز * لمدة 30-60 دقيقة. في السابق ، لتقليل احتمالية حدوث تفاعلات الحساسية ، يُنصح بإعطاء 60-90 مجم من بريدنيزولون عن طريق الوريد.
يتم إعطاء Alteplase عن طريق الوريد بجرعة إجمالية قدرها 100 مجم على النحو التالي: في البداية ، يتم إعطاء 15 مجم من الدواء عن طريق الوريد على شكل جرعة ، ثم يتم البدء في إعطاء التنقيط الوريدي من alteplase خلال 30 دقيقة التالية بمعدل 0.75 مجم / كجم من ويستمر وزن الجسم ، والتنقيط في الوريد لمدة 60 دقيقة القادمة.إدخال الدواء بمعدل 0.5 مجم / كجم من وزن الجسم.
يتم إعطاء Tenecteplase عن طريق الوريد كحقنة بلعة واحدة بجرعة محسوبة اعتمادًا على وزن المريض: بوزن 60-70 كجم - 35 مجم من الدواء ، بوزن 70-80 مجم - 40 مجم من يتم إعطاء tenecteplase بوزن 80-90 كجم - يتم إعطاؤه 45 مجم من الدواء ، بوزن أكثر من 90 كجم - 50 مجم.
يتم إعطاء Prourokinase (purolase) ، وهو دواء محلي ، عن طريق الوريد (سابقًا ، كان الدواء يذوب في 100-200 مل من الماء المقطر * أو محلول كلوريد الصوديوم متساوي التوتر) وفقًا لنظام "التسريب + التسريب". البلعة هي 2،000،000 وحدة دولية ؛ التسريب اللاحق لـ 4،000،000 وحدة دولية خلال 30-60 دقيقة.
بالمقارنة مع الستربتوكيناز (الجيل الأول من مضادات التخثر) ، و alteplase و reteplase (الجيل الثاني من مضادات التخثر) ، والتي تتطلب التنقيط في الوريد بمرور الوقت ، فإن الراحة في استخدام tenecteplase (الجيل الثالث التخثر) هي أنه يمكن إعطاؤه على شكل بلعة IV. هذا مريح للغاية عند إجراء تحلل الخثرات قبل دخول المستشفى في إعداد فريق الإسعاف.
بشكل غير مباشر ، يتم تقييم فعالية العلاج الحالة للخثرة من خلال درجة الانخفاض في الفترة شارع(بالمقارنة مع شدة الارتفاع الأولي) بعد 90 دقيقة من بدء تناول الدواء الحالة للخثرة. إذا كان الفاصل الزمني شارعانخفض بنسبة 50 ٪ أو أكثر مقارنة بالمستوى الأولي ، ويعتبر أن الجلطة كانت فعالة. تأكيد آخر غير مباشر لفعالية العلاج حال التخثر هو ظهور ما يسمى عدم انتظام ضربات القلب (الانقباضات البطينية المتكررة ، تسرع القلب البطيني البطيء ، نادرا ما يحدث الرجفان البطيني). ومع ذلك ، تجدر الإشارة إلى أن فعالة رسميا دليل غير مباشريؤدي العلاج حال التخثر إلى استعادة تدفق الدم التاجي (وفقًا لتصوير الأوعية التاجية). تبلغ كفاءة ضخ الستربتوكيناز حوالي 50٪ ، ألتيبلاز ، ريتيبلاز * 9 وتينيكتيبلاز - 75-85٪.
إذا كان علاج التخثر غير فعال ، فيمكن النظر في مسألة نقل المريض المصاب بمرض التهاب المفاصل الروماتويدي إلى مستشفى يمكنه إجراء PCI (من أجل الخضوع لما يسمى بـ "إنقاذ" PCI في غضون 12 ساعة من بداية المرض).
في حالة تحلل الخثرات الجهازي الفعال في المريض خلال الـ 24 ساعة القادمة ، ولكن ليس قبل 3 ساعات من بدء إعطاء الدواء الحالة للخثرة ، فمن المستحسن إجراء تصوير الأوعية التاجية ، وإذا لزم الأمر ، إجراء PCI.
من أجل تعزيز تأثير التخثر ومنع إعادة تجلط الشريان التاجي (مع تجلط الدم الفعال) ، يتم استخدام الأدوية المضادة للصفيحات (حمض أسيتيل الساليسيليك وكلوبيدوجريل) والأدوية المضادة للثرومبين. (NFG ، LMWH ، مثبطات العامل Xa).
نظرًا للدور المهم للغاية للصفائح الدموية في التسبب في ACS-ST ، فإن قمع التصاق الصفائح الدموية وتنشيطها وتجميعها هو أحد أهم النقاط الرئيسيةفي علاج هذه الفئة من المرضى. حمض أسيتيل الساليسيليك، يمنع انزيمات الأكسدة الحلقية 1 الصفائح الدموية ، ويعطل تخليق الثرموبوكسان A2 فيها ، وبالتالي ، يمنع بشكل لا رجعة فيه تراكم الصفائح الدموية الناجم عن الكولاجين ، ADP والثرومبين.
حمض أسيتيل الساليسيليك (الأسبرين)كدواء مضاد للصفيحات يوصف للمريض في أسرع وقت ممكن قبل المرض(لا يزال في مرحلة ما قبل المستشفى). يُطلب مضغ جرعة التحميل الأولى البالغة 250 مجم من المريض ؛ ثم ، بجرعة 100 مجم ، يأخذ المريض الأسبرين * بالداخل (ويفضل أن يكون في صورة معوية) مرة واحدة في اليوم لفترة طويلة إلى أجل غير مسمى. يصاحب تعيين الأسبرين * في وقت واحد مع العلاج الحالة للخثرة انخفاض في معدل الوفيات لمدة 35 يومًا بنسبة 23 ٪.
ثينوبيريدين (كلوبيدوجريل).والأكثر فعالية هو إضافة مزيج من الأسبرين * وكلوبيدوجريل إلى العلاج الحالة للخثرة (سواء مع جرعة تحميل من 300-600 مجم من عقار كلوبيدوجريل وبدونها). يؤدي هذا العلاج المضاد للصفيحات المكون من عنصرين إلى انخفاض كبير في وتيرة حدوث مضاعفات خطيرة في القلب والأوعية الدموية بنسبة 20٪ في اليوم الثلاثين من المرض.
الأدوية المضادة للثرومبين (مضادات التخثر).ترتبط جدوى استخدام مضادات التخثر (مثبطات UFH و LMWH والعامل Xa) بالحاجة إلى الحفاظ على المباح ومنع إعادة تجلط الشريان التاجي المرتبط بالاحتشاء بعد عملية تجلط الدم الجهازية الناجحة ؛ منع تكوين الجلطات الجدارية في البطين الأيسر والانصمام الشرياني الجهازي اللاحق ، وكذلك الوقاية من تجلط الأوردة المحتملة في الأطراف السفلية والانصمام الخثاري في فروع الشريان الرئوي.
يعتمد اختيار مضادات التخثر على ما إذا كان قد تم إجراء عملية تجلط الدم الجهازي أم لا ، وإذا كان الأمر كذلك ، فما هو الدواء الذي تم استخدامه.
إذا تم إجراء تحلل الخثرة الجهازي باستخدام الستربتوكيناز ، فإن الدواء المختار بين مضادات التخثر هو مثبط العامل Xa fondaparinux sodium (arixtra *) ، والجرعة الأولى منه هي 2.5 مجم عن طريق الوريد على شكل بلعة ، ثم يتم إعطاؤه تحت الجلد مرة واحدة في اليوم في بجرعة 2 ، 5 مجم لمدة 7-8 أيام. بالإضافة إلى fondaparinux ، يمكن استخدام LMWH enoxaparin sodium مبدئيًا كبلعة في الوريد 30 مجم يليها حقنة أولى تحت الجلد بوزن 1 مجم / كجم من وزن الجسم بفاصل زمني 15 دقيقة. بعد ذلك ، يتم إعطاء enoxaparin sodium تحت الجلد مرتين في اليوم بجرعة 1 مجم / كجم من وزن الجسم لمدة أقصاها 8 أيام.
يمكن أيضًا استخدام UFH كعلاج مضاد للتخثر ، وهو أقل ملاءمة من Enoxaparin و fondaparinux sodium. يعد مسار إعطاء UFH أمرًا مهمًا بشكل أساسي: يجب إعطاؤه حصريًا (!) باعتباره تسريبًا وريديًا مستمرًا من خلال أجهزة الجرعات الخاضعة لسيطرة APTT. الهدف من هذا العلاج هو تحقيق قيمة APTT أكبر بمقدار 1.5-2 مرة من القيمة الأولية. للقيام بذلك ، يتم إعطاء UFH مبدئيًا عن طريق الوريد على شكل بلعة تبلغ 60 وحدة / كجم (ولكن ليس أكثر من 4000 وحدة) ، متبوعًا بالتسريب في الوريد بجرعة 12 وحدة / كجم في الساعة ، ولكن لا تتجاوز 1000 وحدة / ساعة أقل. منتظم (بعد 3 و 6 و 12 و 24 ساعة من بدء التسريب) من خلال مراقبة APTT وضبط جرعة UFH وفقًا لذلك.
إذا تم إجراء تحلل الخثرات الجهازية باستخدام منشط البلازمينوجين النسيجي ، فيمكن استخدام الإينوكسابارين أو الهيبارين غير المجزأ كعلاج مضاد للتخثر.
النترات.النترات العضوية هي أدوية تقلل من نقص تروية عضلة القلب. ومع ذلك ، لا توجد بيانات مقنعة لصالح استخدام النترات في احتشاء عضلة القلب الناجم عن ارتفاع ضغط الدم غير المعقد ، لذلك لم تتم الإشارة إلى استخدامها الروتيني في مثل هذه الحالات. يمكن استخدام النترات في الوريد خلال أول يوم أو يومين من الإصابة باحتشاء عضلة القلب المصحوب بعلامات سريرية لإقفار عضلة القلب المستمر ، مع ارتفاع AH ، مع قصور القلب. الجرعة الأولية للدواء هي 5-10 ميكروغرام / دقيقة ، إذا لزم الأمر ، تزداد بمقدار 10-15 ميكروغرام / دقيقة حتى يتحقق التأثير المطلوب أو يصل ضغط الدم الانقباضي إلى 100 ملم زئبق.
طلب حاصرات بيتافي مرحلة مبكرة من علاج المرضى الذين يعانون من احتشاء عضلة القلب الناجم عن احتقان عضلة القلب (عن طريق تقليل الطلب على الأكسجين في عضلة القلب) ، يساعد ذلك على تقليل نقص تروية عضلة القلب ، والحد من منطقة النخر واحتمالية عدم انتظام ضربات القلب التي تهدد الحياة ، بما في ذلك الرجفان البطيني. في المرضى "المستقرين" الذين لا يعانون من اضطرابات الدورة الدموية (انخفاض ضغط الدم الشرياني ، فشل البطين الأيسر الحاد) ، اضطرابات التوصيل القلبي ، الربو القصبي ، من الممكن إعطاء حاصرات بيتا في الوريد في الساعات الأولى من احتشاء عضلة القلب الناجم عن ارتفاع ضغط الدم ، متبوعًا بالتبديل إلى المداومة عن طريق الفم المدخول. ومع ذلك ، في معظم المرضى ، بعد استقرار حالتهم ، من الأفضل أن يصفوا على الفور حاصرات بيتا (ميتوبرولول ، بيسوبرولول ، كارفيديلول ، بروبرانولول) بالداخل. في هذه الحالة ، في البداية ، يتم وصف حاصرات بيتا بجرعة صغيرة ، مع زيادتها اللاحقة تحت سيطرة ضغط الدم ومعدل ضربات القلب وحالة الدورة الدموية.
مثبطات إيسيجب أن تعطى من اليوم الأول من احتشاء عضلة القلب الناجم عن ارتفاع مقطع ST إلا إذا كان هناك موانع. كابتوبريل ، إنالابريل ، راميبريل ، بيريندوبريل ، زوفينوبريل ، تراندولابريل ، إلخ. صغيرة ، تليها زيادتها تحت سيطرة ضغط الدم ومستويات البوتاسيوم وكرياتينين البلازما إلى الجرعات القصوى التي يمكن تحملها أو حتى الوصول إلى القيم المستهدفة. إذا كان المريض لا يتحمل مثبطات إيس، يمكنك استخدام حاصرات مستقبلات الأنجيوتنسين 2 (فالسارتان ، لوسارتان ، تيلميسارتان ، إلخ). تكون مثبطات الإنزيم المحول للأنجيوتنسين فعالة بشكل خاص في المرضى الذين يعانون من احتشاء عضلة القلب الناجم عن ارتفاع مقطع ST الذين لديهم انخفاض في الكسر القذفي أو ظهرت عليهم علامات فشل القلب في المرحلة المبكرة من المرض.
مضاعفات احتشاء عضلة القلب وعلاجها
قصور القلب الحاد (AHF)هي واحدة من أخطر مضاعفات احتشاء عضلة القلب. يتطور عادةً مع انخفاض حاد في انقباض عضلة القلب البطين الأيسر بسبب منطقة واسعة من نقص التروية أو النخر ، والتي تغطي أكثر من 40 ٪ من عضلة القلب البطين الأيسر. في كثير من الأحيان ، يتطور AHF على خلفية قصور القلب المزمن الموجود سابقًا أو يعقد مسار احتشاء عضلة القلب المتكرر.
تميز بين اثنين الخيارات السريريةدوس:
ركود الدم في الدورة الدموية الرئوية ، أي. الوذمة الرئوية (الخلالية أو السنخية) ؛
صدمة قلبية.
في بعض الأحيان يتم الجمع بين كلا الخيارين. هؤلاء المرضى لديهم أسوأ توقعات سير المرض ، حيث أن معدل الوفيات لديهم يتجاوز 80٪.
وذمة رئويةيتطور بسبب زيادة ضغط الدم في الشعيرات الدموية للدورة الرئوية. هذا يؤدي إلى تدفق بلازما الدم من السرير داخل الأوعية الدموية إلى أنسجة الرئة ، مما يؤدي إلى زيادة ترطيبها. يحدث هذا عادة عندما يرتفع الضغط الهيدروستاتيكي في الشعيرات الدموية في الرئتين إلى 24-26 مم زئبق. ويبدأ في تجاوز قيمة ضغط الدم الورمي. هناك وذمة رئوية خلالي وسنخية.
- مع الوذمة السنخية ، يخترق سائل غني بالبروتين الحويصلات الهوائية ويختلط مع الهواء المستنشق ، ويشكل رغوة ثابتة تملأ الخطوط الجوية، يؤدي إلى تعقيد التنفس بشكل حاد ، ويضعف تبادل الغازات ، ويسبب نقص الأكسجة ، والحماض ، وغالبًا ما ينتهي بوفاة المريض.
تعتمد الصدمة القلبية على الانخفاض الحاد في النتاج القلبي ( مؤشر القلب =<1,8 л/мин в 1 м 2), сопровождающееся выраженным снижением систолического АД =<90 мм рт.ст. (на протяжении не менее 30 мин), что приводит к развитию тяжелой гипоперфузии всех органов и тканей, проявляющейся акроцианозом, олиго- и анурией (<30 мл мочи в 1 ч), гипоксией и метаболическим ацидозом. Одновременно происходит «централизация» кровообращения, при которой за счет компенсаторных механизмов, в первую очередь за счет периферической вазоконстрикции и спазма артериол в поперечно-полосатой мускулатуре, кишечнике, селезенке, печени и др. поддерживается кровообращение только в жизненно важных органах (в головном мозге, сердце и легких). Если централизация кровообращения оказывается не в состоянии обеспечить адекватную перфузию жизненно важных органов и стабилизацию АД, то длительная периферическая вазоконстрикция приводит к нарушению микроциркуляции, возникновению ДВС-синдрома, развитию ишемических некрозов в почках, кишечнике, печени, других органах. В итоге развивается полиорганная недостаточность, приводящая к смерти больного.
اعتمادًا على الصورة السريرية والشدة ، ينقسم AHF في مرضى MI إلى أربع فئات (تصنيف Killip).
الصنف الأول: ضيق التنفس المعتدل ، عدم انتظام دقات القلب الجيوب الأنفية في حالة عدم وجود حشرجة احتقانية في الرئتين.
الفئة الثانية: حشرجة فقاعية رطبة غير منفذة في الأجزاء السفلية من الرئتين وليس فوق شفرات الكتف ، مثيرة<50% поверхности легких (интерстициальный отек легких).
الفئة الثالثة: حشرجة فقاعية رطبة غير منفذة ، تغطي أكثر من 50٪ من سطح الرئتين (الوذمة الرئوية السنخية).
الفئة الرابعة: صدمة قلبية.
لعلاج فئة AHF I-II وفقًا لـ Killip ، استخدم:
استنشاق الأكسجين من خلال قناع الوجه أو من خلال القسطرة الأنفية تحت سيطرة تشبع الدم بالأكسجين ؛
إعطاء الحقن الوريدي لمدرات البول العروية (فوروسيميد) بجرعة 20-40 مجم بفاصل 1-4 ساعات ، حسب الحاجة ؛
التسريب الوريدي للنترات (النتروجليسرين ، ثنائي نترات إيزوسوربيد) بجرعة أولية من 3-5 مجم / ساعة في حالة عدم وجود انخفاض ضغط الدم الشرياني ؛
مثبطات الإنزيم المحول للأنجيوتنسين بالداخل في حالة عدم وجود انخفاض ضغط الدم الشرياني ونقص حجم الدم والفشل الكلوي.
يتبع علاج مرضى AHF class III وفقًا لـ Killip الهدف التالي: تحقيق انخفاض في ضغط الإسفين في الشريان الرئوي<20 мм рт.ст. и увеличения сердечного индекса >\ u003d 2.1 لتر / دقيقة في 1 م 2 والتي يتم تنفيذها على النحو التالي:
إعطاء الحقن الوريدي لمدرات البول العروية (فوروسيميد) بجرعة 60-80 مجم أو أكثر على فترات من 1-4 ساعات ، اعتمادًا على إدرار البول ؛
المسكنات المخدرة: المورفين عن طريق الوريد (هيدروكلوريد المورفين *) 1٪ ، 1.0 مل لكل 20.0 مل من محلول كلوريد الصوديوم متساوي التوتر ؛
في حالة عدم وجود انخفاض ضغط الدم الشرياني (BP> 100 مم زئبق) ، التسريب الوريدي لموسعات الأوعية المحيطية (النتروجليسرين أو ثنائي نترات إيزوسوربيد بجرعة ابتدائية من 3-5 مجم / ساعة ، متبوعة بالتصحيح) تحت سيطرة ضغط الدم ومعايير الدورة الدموية المركزية ؛
في وجود انخفاض ضغط الدم الشرياني (BP =<90ммрт.ст.)внутривенная инфузия инотропных препаратов — добутамина, допамина (начальная доза 2,5 мкг/кг в 1 мин с последующей коррекцией) под контролем АД и показателей центральной гемодинамики;
يتبع علاج المرضى المصابين بالفئة الرابعة من AHF وفقًا لـ Killip نفس الهدف كما هو الحال في المرضى الذين يعانون من AHF من الدرجة الثالثة وفقًا لـ Killip ، والذي يتم تنفيذه على النحو التالي:
العلاج بالأكسجين ومراقبة تشبع الأكسجين في الدم وقيمة الأس الهيدروجيني ؛
مع انخفاض في pO 2 أقل من 50 ٪ - التهوية غير الغازية (قناع الوجه ، CIPAP ، BiPAP) أو التهوية الغازية (التنبيب الرغامي) ؛
مراقبة التحكم في معاملات الدورة الدموية المركزية باستخدام قسطرة البالون العائم Swan-Ganz ؛
التسريب الوريدي للأدوية المؤثرة في التقلص العضلي - الدوبوتامين ، الدوبامين (الجرعة الأولية 2.5 ميكروغرام / كغ لكل دقيقة ، يتبعها التصحيح) تحت سيطرة ضغط الدم وديناميكا الدم المركزية ؛
معاكسة البالون داخل الأبهر ؛
إعادة التوعي السريع في عضلة القلب (PCI أو تطعيم المجازة التاجية).
معاكسة النبض بالبالون داخل الأبهر- إحدى طرق المساعدة على الدورة الدموية. يكمن جوهرها في حقيقة أنه في الجزء النازل من الشريان الأورطي (من مستوى أصل الوريد تحت الترقوة الأيسر إلى مستوى منشأ الشرايين الكلوية) ، يتم إدخال قسطرة بالون خاصة عبر الشريان الفخذي عن طريق ثقب ، وهي متصلة بمضخة خاصة تنفخ وتفرغ القسطرة البالونية بشكل متزامن مع نشاط القلب. أثناء الانبساط ، تنتفخ القسطرة البالونية وتسد الشريان الأورطي الهابط. يؤدي هذا إلى زيادة الضغط الانبساطي بشكل كبير في الشريان الأورطي الصاعد وفي جيوب فالسالفا ، مما يؤدي إلى زيادة تدفق الدم التاجي ، والذي يحدث بشكل رئيسي في الانبساط. أثناء الانقباض ، تنكمش القسطرة البالونية بسرعة ، مما يؤدي إلى انخفاض الضغط في الشريان الأورطي الهابط وانخفاض مقاومة طرد الدم من البطين الأيسر. في الوقت نفسه ، ينخفض أيضًا طلب الأكسجين في عضلة القلب. بمساعدة النبض المعاكس للبالون داخل الأبهر ، في بعض المرضى الذين يعانون من الصدمة القلبية ، من الممكن تحسين ديناميكا الدم ، وكسب الوقت ، وإعداد المريض لإعادة تكوين الأوعية الدموية في عضلة القلب.
بالإضافة إلى ذلك ، من الأدوية في علاج الصدمة القلبية ، يتم استخدام محاليل ديكستران في الوريد (بولي جلوسين *. ريوبوليجلوسين *) (أو ديكسترانس آخر) وجلوكوكورتيكويدات ، يتم تصحيح توازن القاعدة الحمضية والكهارل. ومع ذلك ، فإنها تؤثر على الآليات الثانوية للإمراض ولا يمكنها القضاء على الصدمة حتى يتم حل المهمة الرئيسية - استعادة وظيفة ضخ القلب.
الكلمات الدالة
شرط
هدف.لتقييم تطبيق معايير تشخيص احتشاء عضلة القلب في الممارسة السريرية الحقيقية.
المواد والأساليب. أجريت الدراسة من نوفمبر إلى ديسمبر 2011. تاريخ حالة 67 حالة وفاة في قسم أمراض القلب بالمستشفى السريري الذي يحمل اسم ن. ريال سعودى. مرضى صنع السلام في 2009-2010. بمساعدة التحليل غير البارامترى أحادي البعد تم تقييم العلاقة بين جميع الخصائص المدروسة.
نتائج. تم تحليل تاريخ حالة 67 مريضًا ماتوا في وحدة العناية المركزة بقسم أمراض القلب في سن 39 إلى 90 عامًا (متوسط العمر 76 عامًا). ومن بين هؤلاء 33 رجلاً (49٪) و 34 امرأة (51٪). كان 21 شخصًا (31٪) في القسم أقل من سرير واحد في اليوم ، و 46 شخصًا (69٪) - أكثر من سرير واحد في اليوم. تم قبول جميع المرضى على وجه السرعة. تمت إحالة 56 شخصًا (83٪) بواسطة سيارة إسعاف ، شخصان (3٪) من المستوصف ، 4 أشخاص (6٪) من قبل رئيس القسم ، شخص واحد (2٪) استئناف شخصي ، 4 أشخاص (6٪) من أقسام العيادة الأخرى. عيادة احتشاء عضلة القلب الحاد لديها 100٪ من المرضى. وفقًا لنتائج تسجيل مخطط كهربية القلب ، في 47 مريضًا (70 ٪) كان من الممكن تحديد موضع الاحتشاء ، ولم يكن ذلك ممكنًا في البقية (بسبب التغيرات الندبية الواضحة ، LBBB). في 24 شخصًا (36٪) ، كانت هناك آفة في الجدار الخلفي للبطين الأيسر ، لدى 40 شخصًا (60٪) - الجدار الأمامي ، في 22 شخصًا (33٪) - المنطقة القمية و / أو الجانبية. كان لدى معظم المرضى مشاركة في عضلة القلب في أكثر من منطقة واحدة. ارتبط استخدام المؤشرات الحيوية للنخر في التشخيص (CPK-MB وإجمالي CPK) بشكل كبير مع مدة الاستشفاء (p = 0.02). كانت نتائج الدراسات متاحة في 9 مرضى (13٪) ماتوا خلال اليوم الأول من العلاج بالمستشفى و 33 (49٪) قضوا أكثر من يوم في المستشفى. في الوقت نفسه ، غابت نتائج هذه الدراسات لدى 13 مريضًا (19٪) كانوا في المستشفى لأكثر من 24 ساعة. في 40 مريضًا (58٪) ، كانت الزيادة في CPK-MB مهمة تشخيصيًا ، ولكن في مريضين (3٪) ، لم تصل المؤشرات إلى قيم عتبة التشخيص. علاوة على ذلك ، تم تشخيص الاحتشاء الحاد في 27 مريضًا (68٪) بمستوى عالٍ من CPK-MB ، ومريضان (3٪) بقيم طبيعية لهذا المؤشر ، و 20 مريضًا (29٪) دون تناول احسب هذا المعيار (بسبب عدم وجود نتائج الاختبار).). كانت نتائج DECHOCG متاحة فقط في 11 مريضًا (15 ٪). في جميع الحالات ، كانت هناك مناطق من نقص الحركة و / أو عدم الحركة ، ومع ذلك ، كان لدى كل هؤلاء المرضى تاريخ من احتشاء واحد على الأقل لعضلة القلب. تم تشخيص احتشاء عضلة القلب الحاد في 65 مريضاً ، وكان مريضان فقط مصابين بمتلازمة الشريان التاجي الحادة. في المجموع ، تم إجراء تشريح الجثة في 57 حالة. وفقًا لنتائج تشريح الجثة ، لم يتم تأكيد تشخيص احتشاء عضلة القلب الحاد لدى مريضين. في المريض الأول ، عند إرساله للتشريح ، تم تشخيص احتشاء عضلة القلب الحاد دون توطين ، وتم الكشف عن سرطان الرئة الأولي. كان لديه زيادة كبيرة في مستوى CPK-MB (في 3 عينات من أصل 3 مأخوذة) ، لم تكن هناك تغييرات في ECG ، لم يتم تنفيذ DEHOKG. في الحالة الثانية ، كان تشخيص الإحالة هو متلازمة الشريان التاجي الحادة ، وتم الكشف عن التهاب رئوي مدمر في الجانب الأيسر. كان لديه أيضًا زيادة كبيرة في مستوى CPK-MB ، وكانت هناك تغييرات واضحة في ECG ، ومناطق نقص الحركة وفقًا لنتائج DEHOCG. تزامن التوطين الأمامي للاحتشاء مع نتائج تشريح الجثة في 100 ٪ من الحالات ، ولم يتم تأكيد التشخيص الخلفي إلا في 50 ٪ (في 4 مرضى (11 ٪) ، وفي 14 (37 ٪) ، على العكس من ذلك) ، تم تشخيصه). لم تكن هناك علاقة ذات دلالة إحصائية بين التقييم السريري ونتائج تشريح الجثة للآفات في منطقة الحاجز القمي ، وكذلك الآفات في المنطقة الجانبية (p = 0.18 و p = 0.5 ، على التوالي).
خاتمة.لا يتطابق الاستخدام الفعلي لمعايير تشخيص احتشاء عضلة القلب الحاد دائمًا مع المعايير الموصى بها. الأسهل هو تشخيص احتشاء أمامي. تنشأ أكبر الصعوبات عند توطين المنطقة المصابة في منطقة الحاجز القمي و / أو المنطقة الجانبية.