يعتمد اسم المركب على الكلمة الجذرية التي تشير إلى هيدروكربون مشبع بنفس عدد ذرات السلسلة الرئيسية (على سبيل المثال، met-، et-. pro p-، ولكن-، pent-، hex-، إلخ. ). ويلي ذلك لاحقة تميز درجة التشبع، - إذا لم يكن للجزيء روابط متعددة، - إذا كانت هناك روابط مزدوجة و -ni للروابط الثلاثية، على سبيل المثال، بنتان، بنتين. إذا كان هناك عدة روابط متعددة في الجزيء، فإن اللاحقة تشير إلى عدد هذه الروابط، على سبيل المثال: -diene، -triene، وبعد اللاحقة يجب الإشارة إلى موضع الرابطة المتعددة بالأرقام العربية (على سبيل المثال، البيوتين -1، بيوتين-2، بيوتادين-1،3):
CH 3 -CH 2 -CH=CH 2 CH 3 -CH=CH-CH 3 CH 2 =CH-CH=CH 2
بيوتين-1 بيوتين-2 بيوتادين-1,3
بعد ذلك، تحتوي اللاحقة على اسم أقدم مجموعة مميزة في الجزيء، مما يشير إلى موقعها برقم. يتم تعيين البدائل الأخرى باستخدام البادئات. علاوة على ذلك، يتم سردها ليس حسب الأقدمية، ولكن أبجديا. تتم الإشارة إلى موضع البديل برقم قبل البادئة، على سبيل المثال: 3-ميثيل؛ 2-الكلورو الخ إذا كان للجزيء عدة بدائل متطابقة، فسيتم الإشارة إلى عددها قبل اسم المجموعة المقابلة (على سبيل المثال، ثنائي ميثيل، ثلاثي كلورو، وما إلى ذلك). يتم فصل جميع الأرقام في أسماء الجزيئات عن الكلمات بواصلة، وعن بعضها البعض بفواصل. الجذور الهيدروكربونية لها أسماء خاصة بها.
الجذور الهيدروكربونية المشبعة:
ميثيل إيثيل بروبيل الأيزوبروبيل
بوتيل سيك-بوتيل
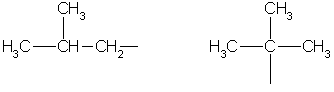
إيزوبوتيل ثالثي بوتيل
الجذور الهيدروكربونية غير المشبعة:
CH 2 = CH- HC - C- CH 2 = CH-CH 2 -
الفينيل إيثينيل أليل
الجذور الهيدروكربونية العطرية:

فينيل بنزين
لنأخذ العلاقة التالية كمثال:

اختيار السلسلة لا لبس فيه، لذلك، جذر الكلمة مكبوت، تليها اللاحقة -en، مما يدل على وجود رابطة متعددة؛ يضمن ترتيب الترقيم أن المجموعة الأقدم (-OH) تحتوي على أصغر رقم؛ وينتهي الاسم الكامل للمركب بلاحقة تشير إلى مجموعة كبار(في هذه الحالة، تشير اللاحقة –o l إلى وجود مجموعة الهيدروكسيل)؛ تتم الإشارة إلى موضع الرابطة المزدوجة ومجموعة الهيدروكسيل بالأرقام.
لذلك، يسمى المركب المعطى penten-4-ol-2.
التسميات التافهة هي مجموعة من الأسماء غير المنتظمة المثبتة تاريخيًا للمركبات العضوية (على سبيل المثال: الأسيتون، وحمض الأسيتيك، والفورمالدهيد، وما إلى ذلك). يتم تقديم أهم الأسماء التافهة في النص عند النظر في فئات المركبات المقابلة.
تسمح التسميات المنطقية بأن يعتمد اسم المادة على بنيتها، مع اختيار مركب أبسط كنموذج أولي. توضح الأمثلة التالية طريقة هذا البناء:
حمض ثلاثي ميثيل ميثان أسيتيل أسيتون فينيل أسيتيك
تصنيف المواد العضوية أكثر تعقيدًا. ويرجع ذلك إلى عدد من الأسباب: الوفرة الشديدة للمركبات العضوية، وتعقيد وتنوع بنيتها، وتاريخ دراسة مركبات الكربون.في الواقع، حتى منتصف القرن التاسع عشر. بدت الكيمياء العضوية، بالتعبير المجازي لـ F. Wöhler*، وكأنها "غابة كثيفة مليئة بالأشياء المدهشة، غابة لا حدود لها لا يمكنك الخروج منها، ولا تجرؤ على اختراقها". فقط مع ظهور النظرية في عام 1861 التركيب الكيميائيالمركبات العضوية "الغابات الكثيفة"
الكيمياء العضويةبدأت تتحول إلى غمرت المياه ضوء الشمسحديقة عادية بها شبكة صارمة من الأزقة والمسارات. كان مؤلفو هذه النظرية ثلاثيًا عالميًا بارزًا من علماء الكيمياء: مواطننا إيه إم بتليروف**، والألماني إف إيه كيكولي، والإنجليزي إيه كوبر.
أرز. 5. فريدريش فولر
(1800–1882)

أرز. 6. الكسندر
ميخائيلوفيتش بتلروف
(1828–1886)
يمكن صياغة جوهر نظرية التركيب الكيميائي التي ابتكروها في شكل ثلاث افتراضات.
1. ترتبط الذرات في الجزيئات بترتيب معين حسب تكافؤها، والكربون في المركبات العضوية رباعي التكافؤ.
2. يتم تحديد خصائص المواد ليس فقط من خلال التركيب النوعي والكمي للعناصر، ولكن أيضًا من خلال ترتيب اتصالات الذرات في الجزيئات، أي. التركيب الكيميائي.
3. الذرات الموجودة في الجزيئات لها تأثير متبادل على بعضها البعض مما يؤثر على خواص المواد.
* كيميائي ألماني. قام بأبحاث في مجال الكيمياء العضوية وغير العضوية. أثبت وجود ظاهرة الأيزومرية وقام لأول مرة بتخليق مادة عضوية (اليوريا) من مادة غير عضوية. تلقى بعض المعادن (الألومنيوم والبريليوم وغيرها).
** كيميائي روسي بارز، مؤلف النظرية الكيميائية
هيكل المواد العضوية. مرتكز علىوقد أوضحت مفاهيم البنية ظاهرة الأيزومرية، وتنبأت بوجود أيزومرات عدد من المواد وقامت بتصنيعها لأول مرة. وكان أول من قام بتركيب مادة سكرية. مؤسس مدرسة الكيمياء الروسيةIkov، والتي ضمت V. V. Markovnikov، A. M. Zaitsev، E. E. Vagner، A. E. Favorsky وآخرون.
اليوم، يبدو من غير المعقول أنه حتى منتصف القرن التاسع عشر، خلال فترة الاكتشافات العظيمة في العلوم الطبيعية، لم يكن لدى العلماء سوى القليل من الفهم للبنية الداخلية للمادة. وكان بتليروف هو الذي أدخل مصطلح "التركيب الكيميائي" ويعني به نظام الروابط الكيميائية بين الذرات في الجزيء، الترتيب المتبادلفي الفضاء. وبفضل هذا الفهم لبنية الجزيء، أصبح من الممكن تفسير ظاهرة الأيزومرية، والتنبؤ بوجود أيزومرات غير معروفة، وربط خواص المواد ببنيتها الكيميائية. لتوضيح ظاهرة الأيزومرية، نقدم صيغ وخصائص مادتين - الكحول الإيثيلي والإيثر ثنائي الميثيل، اللتين لهما نفس التركيب العنصري C2H6O، ولكن في التركيب الكيميائي المختلف (الجدول 2).
الجدول 2
رسم توضيحي لاعتماد خصائص المادةمن هيكلها

تعتبر ظاهرة الأيزومرية المنتشرة بشكل كبير في الكيمياء العضوية أحد أسباب تنوع المواد العضوية. سبب آخر لتنوع المواد العضوية هو القدرة الفريدة لذرة الكربون على تكوين روابط كيميائية مع بعضها البعض، مما ينتج عنه سلاسل الكربون
ذات أطوال وهياكل مختلفة: غير متفرعة، متفرعة، مغلقة. على سبيل المثال، يمكن لأربع ذرات كربون أن تشكل سلاسل كالتالي:

إذا أخذنا في الاعتبار أنه بين ذرتي الكربون يمكن أن توجد ليس فقط روابط C-C بسيطة (مفردة)، ولكن أيضًا مزدوجة C=C وثلاثية C≡C، فإن عدد متغيرات سلاسل الكربون، وبالتالي، العضوية المختلفة المواد تزيد بشكل كبير.
يعتمد تصنيف المواد العضوية أيضًا على نظرية بتليروف للتركيب الكيميائي. اعتمادا على الذرات العناصر الكيميائيةهي جزء من جزيئات جميع المجموعات العضوية: الهيدروكربونات والمركبات المحتوية على الأكسجين والمركبات المحتوية على النيتروجين.
الهيدروكربونات هي مركبات عضوية تتكون فقط من ذرات الكربون والهيدروجين.
بناءً على بنية سلسلة الكربون ووجود أو عدم وجود روابط متعددة فيها، تنقسم جميع الهيدروكربونات إلى عدة فئات. يتم عرض هذه الفئات في الرسم البياني 2.
إذا لم يحتوي الهيدروكربون على روابط متعددة ولم تكن سلسلة ذرات الكربون مغلقة، فهو كما تعلم ينتمي إلى فئة الهيدروكربونات المشبعة، أو الألكانات. جذر هذه الكلمة عربي الأصل، واللاحقة -an موجودة في أسماء جميع الهيدروكربونات من هذه الفئة.
المخطط 2
تصنيف الهيدروكربونات

إن وجود رابطة مزدوجة واحدة في جزيء الهيدروكربون يسمح بتصنيفه على أنه ألكين، ويتم التأكيد على علاقته بهذه المجموعة من المواد
لاحقة -en في الاسم. أبسط الألكين هو الإيثيلين، الذي له الصيغة CH2=CH2. يمكن أن يكون هناك رابطتين مزدوجتين C=C في الجزيء، وفي هذه الحالة، تنتمي المادة إلى فئة القلويات.
حاول شرح معنى اللواحق -diene. على سبيل المثال، 1,3 بوتادين له الصيغة البنائية: CH2=CH–CH=CH2.
تسمى الهيدروكربونات التي تحتوي على رابطة ثلاثية بين الكربون والكربون في الجزيء بالألكينات. تشير اللاحقة -in إلى أن المادة تنتمي إلى هذه الفئة. سلف فئة الألكينات هو الأسيتيلين (الإيثين)، وصيغته الجزيئية هي C2H2، والصيغة الهيكلية هي HC≡CH. من مركبات ذات سلسلة كربون مغلقة
أهم الذرات هي الأرينات - فئة خاصة من الهيدروكربونات، اسم الممثل الأول الذي سمعته على الأرجح هو البنزين C6H6، وصيغته البنائية معروفة أيضًا لكل شخص ثقافي:

كما فهمت بالفعل، بالإضافة إلى الكربون والهيدروجين، يمكن أن تحتوي المواد العضوية على ذرات عناصر أخرى، وخاصة الأكسجين والنيتروجين. في أغلب الأحيان، تشكل ذرات هذه العناصر في مجموعات مختلفة مجموعات تسمى وظيفية.
المجموعة الوظيفية هي مجموعة من الذرات التي تحدد أكثر الخصائص المميزة الخواص الكيميائيةالمادة وانتمائها إلى فئة معينة من المركبات.
يتم عرض الفئات الرئيسية للمركبات العضوية التي تحتوي على مجموعات وظيفية في المخطط 3.
المخطط 3
الفئات الرئيسية للمواد العضوية التي تحتوي على مجموعات وظيفية

المجموعة الوظيفية –OH تسمى الهيدروكسيل وتحدد العضوية في واحدة من أهم فئات المواد العضوية – الكحولات.
يتم تشكيل أسماء الكحوليات باستخدام اللاحقة -ol. على سبيل المثال، الممثل الأكثر شهرة للكحول هو الإيثانولأو الإيثانول C2H5OH.
يمكن ربط ذرة الأكسجين بذرة الكربون بواسطة رابطة كيميائية مزدوجة. تسمى المجموعة >C=O بالكربونيل. مجموعة الكربونيل هي جزء من عدة
المجموعات الوظيفية، بما في ذلك الألدهيد والكربوكسيل. تسمى المواد العضوية التي تحتوي على هذه المجموعات الوظيفية الألدهيدات والأحماض الكربوكسيلية على التوالي. أشهر ممثلي الألدهيدات هم الفورمالديهايد HCOH والأسيتالديهيد CH3SON. مع حمض الاسيتيكربما يكون CH3COOH، الذي يسمى محلوله خل المائدة، مألوفًا لدى الجميع. من السمات الهيكلية المميزة للمركبات العضوية المحتوية على النيتروجين، وقبل كل شيء الأمينات والأحماض الأمينية، وجود المجموعة الأمينية –NH2 في جزيئاتها.
التصنيف أعلاه للمواد العضوية هو أيضًا نسبي جدًا. مثلما يمكن أن يحتوي جزيء واحد (على سبيل المثال، الألكاديين) على رابطتين متعددتين، يمكن أن تحتوي المادة على مجموعتين وظيفيتين أو أكثر. لذا، الوحدات الهيكليةالناقلات الرئيسية للحياة على الأرض - جزيئات البروتين - هي الأحماض الأمينية. تحتوي جزيئات هذه المواد بالضرورة على مجموعتين وظيفيتين على الأقل - مجموعة الكربوكسيل والأمينية. أبسط حمض أميني يسمى الجلايسين وله الصيغة:

مثل هيدروكسيدات مذبذبة، تجمع الأحماض الأمينية بين خصائص الأحماض (بسبب مجموعة الكربوكسيل) والقواعد (بسبب وجود مجموعة أمينية في الجزيء).
بالنسبة لتنظيم الحياة على الأرض، فإن الخصائص المذبذبة للأحماض الأمينية لها أهمية خاصة - بسبب تفاعل المجموعات الأمينية ومجموعات الكربوكسيل من الأحماض الأمينية.
ترتبط الكثير في سلاسل البوليمر من البروتينات.
؟ 1. ما هي الأحكام الرئيسية لنظرية التركيب الكيميائي لـ A.M.بتليروف. ما الدور الذي لعبته هذه النظرية في تطور الكيمياء العضوية؟
2. ما هي فئات الهيدروكربونات التي تعرفها؟ وعلى أي أساس تم هذا التصنيف؟
3. ما هي المجموعة الوظيفية للمركب العضوي؟ ما هي المجموعات الوظيفية التي يمكنك تسميتها؟ ما هي فئات المركبات العضوية التي تحتوي على المجموعات الوظيفية المسماة؟ اكتبه الصيغ العامةفئات المركبات وصيغ ممثليها.
4. حدد الأيزومرية، واكتب صيغ الأيزومرات المحتملة للمركبات ذات التركيبة C4H10O. باستخدام مصادر المعلومات المختلفة، قم بتسمية كل منها وأعد تقريرًا عن أحد المركبات.
5. تصنيف المواد التي صيغها: C6H6، C2H6، C2H4، HCOOH، CH3OH، C6H12O6، إلى أصناف المركبات العضوية المقابلة لها. باستخدام مصادر المعلومات المختلفة، قم بتسمية كل منها وأعد تقريرًا عن أحد المركبات.
6. الصيغة الهيكلية للجلوكوز:  إلى أي فئة من المركبات العضوية تصنف هذه المادة؟ لماذا يسمى مركب ثنائي الوظيفة؟
إلى أي فئة من المركبات العضوية تصنف هذه المادة؟ لماذا يسمى مركب ثنائي الوظيفة؟
7. قارن بين المركبات العضوية وغير العضوية المذبذبة.
8. لماذا تصنف الأحماض الأمينية على أنها مركبات ذات وظائف مزدوجة؟ ما هو الدور الذي تلعبه هذه الميزة الهيكلية للأحماض الأمينية في تنظيم الحياة على الأرض؟
9. إعداد رسالة حول موضوع "الأحماض الأمينية - "لبنات بناء" الحياة" باستخدام الإنترنت.
10. أعط أمثلة على نسبية تقسيم المركبات العضوية إلى فئات معينة. ارسم أوجه تشابه مع النسبية المماثلة للمركبات غير العضوية.
أبسط تصنيف هو هذا. التي تنقسم إليها جميع المواد المعروفة غير العضوية والعضوية. تشمل المواد العضوية الهيدروكربوناتومشتقاتها. جميع المواد الأخرى غير عضوية.

لا المواد العضوية حسب التكوين يتم تقسيمها إلى بسيطة ومعقدة.

مواد بسيطةتتكون من ذرات عنصر كيميائي واحد وتنقسم إلى فلزات ولا فلزات وغازات خاملة. تتكون المواد المعقدة من ذرات عناصر مختلفة مرتبطة ببعضها البعض كيميائيا.
تنقسم المواد غير العضوية المعقدة حسب تركيبها وخصائصها إلى أهم الفئات التالية: أكاسيد ، قواعد ، أحماض ، هيدروكسيدات مذبذبة ، أملاح.
- أكاسيد- وهي مواد معقدة تتكون من عنصرين كيميائيين أحدهما الأكسجين ذو حالة الأكسدة (-2). الصيغة العامة للأكاسيد هي: E m O n، حيث m هو عدد ذرات العنصر E، و n هو عدد ذرات الأكسجين. وتصنف الأكاسيد بدورها إلى مكونة للملح وغير مكونة للملح. تنقسم المركبات المكونة للملح إلى قاعدية، ومذبذبة، وحمضية، والتي تتوافق مع القواعد، والهيدروكسيدات المذبذبة، والأحماض، على التوالي.
- أكاسيد أساسيةهي أكاسيد فلزية في حالات الأكسدة +1 و +2. وتشمل هذه:
- أكاسيد المعادن من المجموعة الفرعية الرئيسية للمجموعة الأولى ( الفلزات القلوية) لى الاب
- أكاسيد المعادن من المجموعة الفرعية الرئيسية للمجموعة الثانية ( Mg والمعادن الأرضية القلوية) ملغ-رع
- أكاسيد المعادن الانتقالية في حالات الأكسدة المنخفضة
- أكاسيد حمضية- تشكل اللافلزات مع ثاني أكسيد الكربون. أكثر من +2 والمعادن مع S.O. من +5 إلى +7 (SO 2، SeO 2، P 2 O 5، As 2 O 3، CO 2، SiO 2، CrO 3 و Mn 2 O 7). استثناء: لا أكاسيد 2 و ClO 2 لا توجد هيدروكسيدات حمضية مقابلة، لكنها تعتبر حمضية.
- أكاسيد مذبذبة- تتكون من معادن مذبذبة تحتوي على S.O. +2، +3، +4 (BeO، Cr 2 O 3، ZnO، Al 2 O 3، GeO 2، SnO 2 و PbO).
- أكاسيد غير ملحية- أكاسيد غير معدنية مع CO +1، +2 (CO، NO، N 2 O، SiO).
- الأسباب- هذه مواد معقدة تتكون من ذرات معدنية ومجموعة هيدروكسيل واحدة أو أكثر (-OH). الصيغة العامة للقواعد: M(OH) y، حيث y هو عدد مجموعات الهيدروكسيد، يساوي الدرجةأكسدة المعدن M (عادة +1 و +2). وتنقسم القواعد إلى قابلة للذوبان (قلويات) وغير قابلة للذوبان.
- الأحماض-(هيدروكسيدات الحمض) هي مواد معقدة تتكون من ذرات هيدروجين يمكن استبدالها بذرات معدنية وبقايا حمضية. الصيغة العامة للأحماض: H x Ac، حيث Ac هي البقايا الحمضية (من "الحمض" الإنجليزي - الحمض)، x هو عدد ذرات الهيدروجين المساوية لشحنة أيون البقايا الحمضية.
- هيدروكسيدات مذبذبة- هذه مواد معقدة تظهر خواص الأحماض وخواص القواعد. ولذلك، يمكن كتابة صيغ هيدروكسيدات مذبذبة في كل من شكل حمض وقاعدة.
- أملاح- هذه مواد معقدة تتكون من الكاتيونات المعدنية والأنيونات من بقايا الأحماض. وينطبق هذا التعريف على الأملاح المتوسطة.
- أملاح متوسطة- هذه هي منتجات الاستبدال الكامل لذرات الهيدروجين في جزيء حمض بذرات معدنية أو الاستبدال الكامل لمجموعات الهيدروكسيد في جزيء أساسي بمخلفات حمضية.
- أملاح حمضية- يتم استبدال ذرات الهيدروجين الموجودة في الحمض جزئيًا بذرات المعدن. يتم الحصول عليها عن طريق تحييد القاعدة مع وجود فائض من الحمض. لتسمية بشكل صحيح ملح حامض,من الضروري إضافة البادئة hydro- أو dihydro- إلى اسم الملح العادي، وذلك حسب عدد ذرات الهيدروجين الموجودة في الملح الحمضي، على سبيل المثال، KHCO 3 هو بيكربونات البوتاسيوم، KH 2 PO 4 هو أورثوفوسفات ثنائي هيدروجين البوتاسيوم. . ويجب أن نتذكر ذلك أملاح حمضيةيمكن أن يشكل حمضين أساسيين أو أكثر فقط.
- الأملاح الأساسية- يتم استبدال مجموعات الهيدروكسيد القاعدية (OH -) جزئيًا بالمخلفات الحمضية. لتسمية الملح الأساسي,من الضروري إضافة البادئة hydroxo- أو dihydroxo- إلى اسم الملح العادي، اعتماداً على عدد مجموعات OH الموجودة في الملح، فمثلاً (CuOH) 2 CO 3 عبارة عن هيدروكسي كربونات النحاس (II). تذكر أن الأملاح الأساسية لا يمكن أن تشكل إلا قواعد تحتوي على مجموعتين أو أكثر من مجموعات الهيدروكسيد.
- أملاح مزدوجة- تحتوي على كاتيونين مختلفين، ويتم الحصول عليهما عن طريق التبلور من محلول مختلط من الأملاح بكاتيونات مختلفة، ولكن نفس الأنيونات. على سبيل المثال، KAl(SO 4) 2، KNaSO 4.
- أملاح مختلطة- تحتوي على أنيونين مختلفين. على سبيل المثال، Ca(OCl)Cl.
- هيدرات الأملاح (الهيدرات البلورية) - تحتوي على جزيئات ماء متبلورة. مثال: Na 2 SO 4 · 10H 2 O.

تصنيف المواد العضوية
تسمى المركبات التي تتكون من ذرات الهيدروجين والكربون فقط الهيدروكربونات. قبل البدء بهذا القسم، تذكر، لتبسيط التسجيل، فإن الكيميائيين لا يكتبون ذرات الكربون والهيدروجين في سلاسل، لكن لا تنسوا أن الكربون يشكل أربع روابط، وإذا كان الكربون في الشكل متصلاً برابطتين، فهو متصل بذرات الهيدروجين باثنين آخرين، على الرغم من عدم الإشارة إلى الأخير:

اعتمادًا على بنية سلسلة الكربون، تنقسم المركبات العضوية إلى مركبات مفتوحة السلسلة - غير حلقية(الأليفة) و دوري- بسلسلة مغلقة من الذرات.
دوريتنقسم إلى مجموعتين: كربوسيكليةاتصالات و حلقية غير متجانسة.
المركبات الكربونية الحلقية، بدورها، تشمل سلسلتين من الاتصالات: الحلقيةو عطرية.
المركبات العطريةيعتمد التركيب الجزيئي على حلقات مسطحة تحتوي على الكربون مع نظام مغلق خاص من إلكترونات π. تشكيل نظام π مشترك (سحابة إلكترون π واحدة).

يمكن أن تحتوي كل من الهيدروكربونات الحلقية (الأليفاتية) والحلقية على روابط متعددة (مزدوجة أو ثلاثية). تسمى هذه الهيدروكربونات غير محدود(غير مشبعة)، على عكس حد(مشبعة) تحتوي على روابط مفردة فقط.
رابطة باي (رابطة π) هي رابطة تساهمية تتكون من تداخل المدارات الذرية. على عكس روابط سيجما، والتي يتم إنشاؤها من خلال تداخل المدارات الذرية s على طول خط الترابط الذري، يتم تشكيل روابط باي من خلال تداخل المدارات الذرية p على جانبي خط الترابط الذري.
في حالة تكوين نظام عطري، على سبيل المثال البنزين C6H6، تكون كل من ذرات الكربون الست في حالة تهجين sp2 وتشكل ثلاث روابط سيجما بزوايا رابطة 120 درجة. يتم توجيه الإلكترون الرابع من كل ذرة كربون بشكل عمودي على مستوى حلقة البنزين. وبشكل عام تظهر رابطة واحدة تمتد إلى جميع ذرات الكربون في حلقة البنزين. تتشكل منطقتان من روابط pi عالية الكثافة الإلكترونية على جانبي مستوى رابطة سيجما. مع مثل هذه الرابطة، تصبح جميع ذرات الكربون في جزيء البنزين متكافئة، وبالتالي، يكون مثل هذا النظام أكثر استقرارًا من النظام الذي يحتوي على ثلاث روابط مزدوجة موضعية.

تسمى الهيدروكربونات الأليفاتية المشبعة الألكانات؛ ولها الصيغة العامة C n H 2n + 2، حيث n هو عدد ذرات الكربون. غالبًا ما يستخدم اسمها القديم اليوم - البارافينات:
تسمى الهيدروكربونات الأليفاتية غير المشبعة ذات الرابطة الثلاثية الألكينات. صيغتها العامة هي C n H 2n - 2
الهيدروكربونات الحلقية المشبعة هي ألكانات حلقية، صيغتها العامة هي C n H 2n:

نظرنا إلى تصنيف الهيدروكربونات. ولكن إذا كان في هذه الجزيئات واحد أو عدد أكبريتم استبدال ذرات الهيدروجين بذرات أو مجموعات ذرات أخرى (الهالوجينات، مجموعات الهيدروكسيل، المجموعات الأمينية، إلخ)، ويتم تشكيل مشتقات الهيدروكربون: مشتقات الهالوجين، المحتوية على الأكسجين، المحتوية على النيتروجين وغيرها من المركبات العضوية.

تسمى الذرات أو مجموعات الذرات التي تحدد الخصائص الأكثر تميزًا لفئة معينة من المواد بالمجموعات الوظيفية.
تشكل الهيدروكربونات ومشتقاتها التي لها نفس المجموعة الوظيفية سلسلة متجانسة.
السلسلة المتجانسة عبارة عن سلسلة من المركبات التي تنتمي إلى نفس الفئة (المتجانسات)، وتختلف عن بعضها البعض في التركيب بعدد صحيح من مجموعات -CH 2 (فرق متماثل)، ولها بنية مماثلة، وبالتالي خصائص كيميائية مماثلة.
إن تشابه الخواص الكيميائية للمتجانسات يبسط إلى حد كبير دراسة المركبات العضوية.
الهيدروكربونات البديلة
- الهيدروكربونات المهلجنةيمكن اعتبارها منتجات استبدال ذرة هيدروجين واحدة أو أكثر بذرات الهالوجين في الهيدروكربونات. وفقًا لهذا ، قد يكون هناك مشتقات هالوجين أحادية مشبعة وغير مشبعة (بشكل عام ، بولي) الصيغة العامة لمشتقات الهالوجين من الهيدروكربونات المشبعة هي R-G. تشمل المواد العضوية المحتوية على الأكسجين الكحوليات والفينولات والألدهيدات والكيتونات والأحماض الكربوكسيلية والأسترات البسيطة.
- الكحوليات- مشتقات الهيدروكربونات التي يتم فيها استبدال ذرة هيدروجين واحدة أو أكثر بمجموعات الهيدروكسيل، وتسمى الكحولات أحادية الهيدريك إذا كانت تحتوي على مجموعة هيدروكسيل واحدة، ومشبعة إذا كانت من مشتقات الألكانات. كحولات أحادية الهيدريك: ر-أوه.
- الفينولات- مشتقات الهيدروكربونات العطرية (سلسلة البنزين)، حيث يتم استبدال ذرة هيدروجين واحدة أو أكثر في حلقة البنزين بمجموعات الهيدروكسيل.
- الألدهيدات والكيتونات- مشتقات الهيدروكربونات التي تحتوي على مجموعة ذرات الكربونيل (الكربونيل).في جزيئات الألدهيد، ترتبط رابطة كربونيل واحدة بذرة هيدروجين، والأخرى بجذر هيدروكربون. وفي حالة الكيتونات، ترتبط مجموعة الكربونيل باثنتين (بشكل عام) مختلفة) المتطرفين.
- الأثيراتهي مواد عضوية تحتوي على جذرين هيدروكربونيين متصلين بواسطة ذرة أكسجين: R=O-R أو R-O-R 2. يمكن أن تكون الجذور متماثلة أو مختلفة. يتم التعبير عن تكوين الإيثرات بالصيغة C n H 2n +2O.
- استرات- مركبات تتكون من استبدال ذرة الهيدروجين من مجموعة الكربوكسيل فيها الأحماض الكربوكسيليةإلى جذري الهيدروكربون.
- مركبات النيترو- مشتقات الهيدروكربونات التي يتم فيها استبدال ذرة هيدروجين واحدة أو أكثر بمجموعة نيترو -NO 2.
- الأمينات- المركبات التي تعتبر من مشتقات الأمونيا، حيث يتم استبدال ذرات الهيدروجين بجذور هيدروكربونية، وبحسب طبيعة الجذور يمكن أن تكون الأمينات أليفاتية. اعتمادًا على عدد ذرات الهيدروجين التي تم استبدالها بالجذور، يتم التمييز بين الأمينات الأولية والثانوية والثالثية. في حالة معينة، قد يكون للأمينات الثانوية والثالثية نفس الجذور. يمكن أيضًا اعتبار الأمينات الأولية مشتقات من الهيدروكربونات (الألكانات) حيث يتم استبدال ذرة هيدروجين واحدة بمجموعة أمينية. تحتوي الأحماض الأمينية على مجموعتين وظيفيتين متصلتين بجذر الهيدروكربون - المجموعة الأمينية -NH 2 والكربوكسيل -COOH.
ومن المعروف أن المركبات العضوية الهامة الأخرى لها عدة مجموعات وظيفية مختلفة أو متطابقة، وسلاسل خطية طويلة متصلة بحلقات البنزين. في مثل هذه الحالات، يكون التحديد الدقيق لما إذا كانت المادة تنتمي إلى فئة معينة أمرًا مستحيلًا. وغالباً ما يتم تصنيف هذه المركبات إلى مجموعات محددة من المواد: الكربوهيدرات، البروتينات، احماض نوويةوالمضادات الحيوية والقلويدات وما إلى ذلك. حاليًا، تُعرف أيضًا العديد من المركبات التي يمكن تصنيفها على أنها عضوية وغير عضوية. يطلق عليهم مركبات العناصر العضوية. يمكن اعتبار بعضها مشتقات هيدروكربونية.
التسميات
هناك تسميتان تستخدمان لتسمية المركبات العضوية: عقلانية ومنهجية (IUPAC) وأسماء تافهة.

تجميع الأسماء حسب تسميات IUPAC:
1) يعتمد اسم المركب على جذر الكلمة، مما يدل على هيدروكربون مشبع بنفس عدد ذرات السلسلة الرئيسية.
2) تتم إضافة لاحقة إلى الجذر لوصف درجة التشبع:
(نهائي، لا توجد اتصالات متعددة)؛
En (في وجود رابطة مزدوجة)؛
في (في وجود رابطة ثلاثية).

إذا كان هناك عدة روابط متعددة، فإن اللاحقة تشير إلى عدد هذه الروابط (-diene، -triene، وما إلى ذلك)، وبعد اللاحقة يجب الإشارة إلى موضع الرابطة المتعددة بالأرقام، على سبيل المثال:
CH 3 –CH 2 –CH=CH 2 CH 3 –CH=CH –CH 3
بيوتين-1 بيوتين-2
CH 2 = CH – CH = CH2
يتم وضع مجموعات مثل النيترو والهالوجينات والجذور الهيدروكربونية غير المدرجة في السلسلة الرئيسية في البادئة. تم سردها في الترتيب الأبجدي. تتم الإشارة إلى موضع البديل بالرقم الموجود قبل البادئة.
ترتيب التسمية كالتالي:
1. ابحث عن أطول سلسلة من ذرات C.
2. قم بترقيم ذرات الكربون في السلسلة الرئيسية بالتسلسل بدءاً من الطرف الأقرب للفرع.
3. اسم الألكان مكون من أسماء الجذور الجانبية، مرتبة حسب الترتيب الأبجدي، مع الإشارة إلى موقعها في السلسلة الرئيسية، واسم السلسلة الرئيسية.
 الإجراء لتجميع الاسم
الإجراء لتجميع الاسم اللغة الكيميائية، والتي تتضمن الرمزية الكيميائية كأحد الأجزاء الأكثر تحديدًا (بما في ذلك الصيغ الكيميائية)، هي وسيلة نشطة مهمة لتعلم الكيمياء، وبالتالي تتطلب تطبيقًا واضحًا وواعيًا.
الصيغ الكيميائية- هذه صور تقليدية لتركيب وبنية المواد الفردية كيميائيًا باستخدام الرموز والمؤشرات الكيميائية والعلامات الأخرى. عند دراسة التركيب والتركيب الكيميائي والإلكتروني والمكاني للمواد، وخصائصها الفيزيائية والكيميائية، والأيزومرية وغيرها من الظواهر، يتم استخدام الصيغ الكيميائية من أنواع مختلفة.
يتم استخدام العديد من أنواع الصيغ (البسيطة، الجزيئية، الهيكلية، الإسقاطية، المطابقة، وما إلى ذلك) بشكل خاص في دراسة المواد ذات التركيب الجزيئي - معظم المواد العضوية وجزء صغير نسبيًا من المواد غير العضوية في الظروف العادية. يتم استخدام عدد أقل بكثير من أنواع الصيغ (الأبسط) في دراسة المركبات غير الجزيئية، والتي ينعكس هيكلها بشكل أكثر وضوحًا من خلال نماذج الكرة والعصا والرسوم البيانية للهياكل البلورية أو خلايا الوحدة الخاصة بها.

وضع الصيغ البنائية الكاملة والمختصرة للهيدروكربونات
مثال:
كتابة كاملة ومختصرة الصيغ الهيكليةالبروبان C3H8.
حل:
1. اكتب 3 ذرات كربون في خط واربطها بروابط:
س-س-س
2. أضف شرطات (روابط) بحيث تحتوي كل ذرة كربون على 4 روابط:


4. اكتب صيغة هيكلية مختصرة:
CH 3 –CH 2 –CH 3
جدول الذوبان
يتم تصنيف المركبات العضوية مع الأخذ في الاعتبار خاصيتين هيكليتين رئيسيتين:
هيكل سلسلة الكربون (الهيكل العظمي الكربوني)؛
وجود وهيكل المجموعات الوظيفية.
هيكل الكربون (سلسلة الكربون) عبارة عن سلسلة من ذرات الكربون المرتبطة كيميائيًا ببعضها البعض.
المجموعة الوظيفية - ذرة أو مجموعة ذرات تحدد ما إذا كان المركب ينتمي إلى فئة معينة ويكون مسؤولاً عن خواصه الكيميائية.
تصنيف المركبات حسب بنية سلسلة الكربون
اعتمادًا على بنية سلسلة الكربون، تنقسم المركبات العضوية إلى غير حلقية ودورية.
مركبات غير حلقية - مركبات ذات يفتح(مفتوحة) سلسلة الكربون. وتسمى هذه الاتصالات أيضًا الأليفاتية.
من بين المركبات غير الحلقية، يتم التمييز بين المشبعة (المشبعة)، التي تحتوي على وحدات واحدة فقط في الهيكل العظمي. اتصالات CCو غير محدود(غير مشبعة)، بما في ذلك الروابط المتعددة C = C و C C.
مركبات لاحلقية
الحدود:

غير محدود:

وتنقسم المركبات الحلقية أيضًا إلى مركبات غير متفرعة و سلسلة متفرعة. وفي هذه الحالة يؤخذ في الاعتبار عدد روابط ذرة الكربون مع ذرات الكربون الأخرى.
السلسلة، التي تتضمن ذرات الكربون الثلاثية أو الرباعية، متفرعة (غالبًا ما يُشار إلى الاسم بالبادئة "iso").
على سبيل المثال:

ذرات الكربون:
أساسي؛
ثانوي؛
بعد الثانوي.
المركبات الحلقية هي مركبات ذات سلسلة كربون مغلقة.
اعتمادًا على طبيعة الذرات التي تتكون منها الدورة، يتم التمييز بين المركبات الحلقية والحلقية غير المتجانسة.
تحتوي المركبات الحلقية الكربونية على ذرات الكربون فقط في الحلقة. وهي مقسمة إلى مجموعتين لهما خصائص كيميائية مختلفة إلى حد كبير: مركبات حلقية أليفاتية - مركبات حلقية قصيرة - ومركبات عطرية.
المركبات الكربونية الحلقية
أليسليك:

العطرية:

مركبات حلقية غير متجانسة تحتوي في الحلقة، بالإضافة إلى ذرات الكربون، على ذرة واحدة أو أكثر من العناصر الأخرى - ذرات مغايرة(من اليونانية مغاير- أخرى، مختلفة) - الأكسجين، النيتروجين، الكبريت، إلخ.
مركبات حلقية غير متجانسة

تصنيف المركبات حسب المجموعات الوظيفية
تسمى المركبات التي تحتوي على الكربون والهيدروجين فقط بالهيدروكربونات.
يمكن اعتبار المركبات العضوية الأخرى الأكثر عددًا بمثابة مشتقات للهيدروكربونات، والتي تتشكل عن طريق إدخال مجموعات وظيفية تحتوي على عناصر أخرى في الهيدروكربونات.
اعتمادا على طبيعة المجموعات الوظيفية، يتم تقسيم المركبات العضوية إلى فئات. يرد في الجدول بعض المجموعات الوظيفية الأكثر تميزًا وفئات المركبات المقابلة لها:
فئات المركبات العضوية

ملحوظة: تتضمن المجموعات الوظيفية أحيانًا روابط مزدوجة وثلاثية.
قد تحتوي جزيئات المركبات العضوية على مجموعتين وظيفيتين متطابقتين أو مختلفتين أو أكثر.
على سبيل المثال: HO-CH 2 - CH 2 -OH (إيثيلين جلايكول)؛ NH 2 -CH 2 - COOH (حمض أميني الجليكاين).
جميع فئات المركبات العضوية مترابطة. يتم الانتقال من فئة من المركبات إلى أخرى بشكل رئيسي بسبب تحول المجموعات الوظيفية دون تغيير الهيكل الكربوني. تشكل مركبات كل فئة سلسلة متجانسة.
في الماضي، قسم العلماء جميع المواد الموجودة في الطبيعة إلى غير حية ومعيشة مشروطة، بما في ذلك مملكة الحيوانات والنباتات من بين هذه الأخيرة. تسمى مواد المجموعة الأولى بالمعادن. وتلك المدرجة في الثانية بدأت تسمى المواد العضوية.
ماذا يعني هذا؟ فئة المواد العضوية هي الأكثر شمولاً بين الجميع مركبات كيميائيةمعروف لدى العلماء المعاصرين. يمكن الإجابة على سؤال ما هي المواد العضوية بهذه الطريقة - وهي مركبات كيميائية تحتوي على الكربون.
يرجى ملاحظة أنه ليست كل المركبات المحتوية على الكربون عضوية. على سبيل المثال، لا يتم تضمين الكوربيدات والكربونات وحمض الكربونيك والسيانيد وأكاسيد الكربون.
لماذا يوجد الكثير من المواد العضوية؟
الجواب على هذا السؤال يكمن في خصائص الكربون. وهذا العنصر مثير للفضول لأنه قادر على تكوين سلاسل من ذراته. وفي الوقت نفسه، تكون رابطة الكربون مستقرة جدًا.
بالإضافة إلى ذلك، فإنه يظهر في المركبات العضوية تكافؤًا عاليًا (IV)، أي. القدرة على تكوين روابط كيميائية مع مواد أخرى. وليس مفردًا فحسب، بل أيضًا مزدوجًا وحتى ثلاثيًا (المعروف أيضًا باسم المضاعفات). ومع زيادة تعدد الروابط، تصبح سلسلة الذرات أقصر ويزداد استقرار الرابطة.
يتمتع الكربون أيضًا بالقدرة على تكوين هياكل خطية ومسطحة وثلاثية الأبعاد.
وهذا هو سبب تنوع المواد العضوية في الطبيعة. يمكنك بسهولة التحقق من ذلك بنفسك: قف أمام المرآة وانظر بعناية إلى انعكاسك. كل واحد منا هو كتاب مدرسي عن الكيمياء العضوية. فكر في الأمر: ما لا يقل عن 30% من كتلة كل خلية من خلاياك عبارة عن مركبات عضوية. البروتينات التي تبني جسمك. الكربوهيدرات، والتي تعمل بمثابة "الوقود" ومصدر للطاقة. الدهون التي تخزن احتياطيات الطاقة. الهرمونات التي تتحكم في عمل الأعضاء وحتى سلوكك. الانزيمات التي تثير التفاعلات الكيميائيةبداخلك. وحتى "الكود المصدري"، أي سلاسل الحمض النووي، كلها مركبات عضوية قائمة على الكربون.
تكوين المواد العضوية
كما قلنا في البداية، فإن مادة البناء الرئيسية للمواد العضوية هي الكربون. ومن الناحية العملية، يمكن لأي عنصر، عندما يتحد مع الكربون، أن يشكل مركبات عضوية.
في الطبيعة، تحتوي المواد العضوية في أغلب الأحيان على الهيدروجين والأكسجين والنيتروجين والكبريت والفوسفور.
هيكل المواد العضوية
يمكن تفسير تنوع المواد العضوية الموجودة على الكوكب وتنوع بنيتها السمات المميزةذرات الكربون.
تتذكر أن ذرات الكربون قادرة على تكوين روابط قوية جدًا مع بعضها البعض، وتتصل في سلاسل. والنتيجة هي جزيئات مستقرة. تعد الطريقة التي ترتبط بها ذرات الكربون في سلسلة (مرتبة بشكل متعرج) إحدى السمات الرئيسية لبنيتها. يمكن أن يتحد الكربون في سلاسل مفتوحة وسلاسل مغلقة (دورية).
ومن المهم أيضا أن الهيكل المواد الكيميائيةيؤثر بشكل مباشر على خصائصها الكيميائية. إن الطريقة التي تؤثر بها الذرات ومجموعات الذرات في الجزيء على بعضها البعض تلعب أيضًا دورًا مهمًا.
ونظرًا للخصائص الهيكلية، فإن عدد مركبات الكربون من نفس النوع يصل إلى العشرات والمئات. على سبيل المثال، يمكننا أن نعتبر مركبات الكربون الهيدروجينية: الميثان، والإيثان، والبروبان، والبيوتان، وما إلى ذلك.
على سبيل المثال، الميثان - CH 4. هذا المزيج من الهيدروجين والكربون في الظروف العاديةيبقى في حالة غازية مجمعة. عندما يظهر الأكسجين في التركيبة، يتم تشكيل سائل - كحول الميثيل CH 3 OH.
ليس فقط المواد ذات التركيبات النوعية المختلفة (كما في المثال أعلاه) تظهر خصائص مختلفة، ولكن المواد التي لها نفس التركيب النوعي قادرة أيضًا على ذلك. ومن الأمثلة على ذلك القدرة المختلفة للميثان CH 4 والإيثيلين C 2 H 4 على التفاعل مع البروم والكلور. الميثان قادر على مثل هذه التفاعلات فقط عند تسخينه أو تحت الضوء فوق البنفسجي. ويتفاعل الإيثيلين حتى بدون إضاءة أو تدفئة.
لنفكر في هذا الخيار: التركيب النوعي للمركبات الكيميائية هو نفسه، ولكن التركيب الكمي مختلف. ثم تختلف الخواص الكيميائية للمركبات. كما هو الحال مع الأسيتيلين C2H2 والبنزين C6H6.
ليس أقلها دور في هذا التنوع تلعبه خصائص المواد العضوية "المرتبطة" ببنيتها مثل الأيزومرية والتماثل.
تخيل أن لديك مادتين متطابقتين ظاهريًا - نفس التركيب ونفس الصيغة الجزيئية لوصفهما. لكن هيكل هذه المواد يختلف اختلافا جذريا، والذي يتبعه الفرق الكيميائي و الخصائص الفيزيائية. على سبيل المثال، الصيغة الجزيئيةيمكن كتابة C 4 H 10 اثنين مواد مختلفة: البيوتان والأيزوبيوتان.

نحن نتحدث عن نظائر– المركبات التي لها نفس التركيب والوزن الجزيئي. لكن الذرات الموجودة في جزيئاتها مرتبة في ترتيبات مختلفة (بنية متفرعة وغير متفرعة).
بخصوص التماثلهي إحدى خصائص سلسلة الكربون التي يوجد فيها كل منها العضو القادمويمكن الحصول عليه بإضافة مجموعة CH 2 إلى المجموعة السابقة. يمكن التعبير عن كل سلسلة متجانسة بصيغة عامة واحدة. ومعرفة الصيغة، من السهل تحديد تكوين أي من أعضاء السلسلة. على سبيل المثال، يتم وصف متجانسات الميثان بالصيغة C n H 2n+2.
ومع زيادة "الفرق المتماثل" CH 2، تتقوى الرابطة بين ذرات المادة. لنأخذ سلسلة الميثان المتجانسة: أعضاؤه الأربعة الأولى هي الغازات (الميثان، الإيثان، البروبان، البيوتان)، والستة التالية هي السوائل (البنتان، الهكسان، الهيبتان، الأوكتان، النونان، الديكان)، ثم تتبع المواد الموجودة في المادة الصلبة حالة التجميع (بنتاديكان، إيكوسان، الخ). وكلما كانت الرابطة بين ذرات الكربون أقوى، كلما زاد الوزن الجزيئي ونقاط الغليان والانصهار للمواد.
ما هي فئات المواد العضوية الموجودة؟
تشمل المواد العضوية ذات الأصل البيولوجي ما يلي:
- البروتينات.
- الكربوهيدرات.
- احماض نووية؛
- الدهون.
يمكن أيضًا تسمية النقاط الثلاث الأولى بالبوليمرات البيولوجية.
أكثر تصنيف مفصلالمواد الكيميائية العضوية لا تغطي المواد ذات الأصل البيولوجي فقط.
الهيدروكربونات تشمل:
- المركبات اللاحلقية:
- الهيدروكربونات المشبعة (الألكانات)؛
- الهيدروكربونات غير المشبعة:
- الألكينات.
- الألكينات.
- القلاديين.
- اتصالات دورية:
- المركبات الحلقية:
- الحلقية.
- عطرية.
- مركبات حلقية غير متجانسة.
- المركبات الحلقية:
هناك أيضًا فئات أخرى من المركبات العضوية التي يتحد فيها الكربون مع مواد أخرى غير الهيدروجين:
- الكحوليات والفينولات.
- الألدهيدات والكيتونات.
- الأحماض الكربوكسيلية؛
- استرات.
- الدهون.
- الكربوهيدرات:
- السكريات الأحادية.
- السكريات قليلة التعدد؛
- السكريات.
- عديدات السكاريد المخاطية.
- الأمينات.
- أحماض أمينية؛
- البروتينات.
- احماض نووية.
صيغ المواد العضوية حسب الفئة

أمثلة على المواد العضوية
كما تتذكر، في جسم الإنسان أنواع مختلفةالمادة العضوية هي الأساس. هذه هي الأنسجة والسوائل لدينا، والهرمونات والأصباغ، والإنزيمات وATP، وأكثر من ذلك بكثير.
في أجسام البشر والحيوانات، تعطى الأولوية للبروتينات والدهون (نصف الكتلة الجافة للخلية الحيوانية عبارة عن بروتينات). في النباتات (حوالي 80٪ من الكتلة الجافة للخلية) - الكربوهيدرات، في المقام الأول المعقدة - السكريات. بما في ذلك السليلوز (الذي بدونه لن يكون هناك ورق)، والنشا.
دعونا نتحدث عن بعضها بمزيد من التفصيل.
على سبيل المثال، حول الكربوهيدرات. إذا كان من الممكن أخذ وقياس كتل جميع المواد العضوية على هذا الكوكب، فإن الكربوهيدرات هي التي ستفوز في هذه المنافسة.
أنها بمثابة مصدر للطاقة في الجسم وهي مواد بناءللخلايا، وأيضا لتخزين المواد. تستخدم النباتات النشا لهذا الغرض، وتستخدم الحيوانات الجليكوجين.
بالإضافة إلى ذلك، الكربوهيدرات متنوعة للغاية. على سبيل المثال، الكربوهيدرات البسيطة. السكريات الأحادية الأكثر شيوعًا في الطبيعة هي البنتوز (بما في ذلك الريبوز منقوص الأكسجين، وهو جزء من الحمض النووي) والهيكسوز (الجلوكوز، وهو مألوف بالنسبة لك).
مثل الطوب، في موقع بناء كبير من الطبيعة، يتم بناء السكريات من الآلاف والآلاف من السكريات الأحادية. بدونها، على وجه التحديد، بدون السليلوز والنشا، لن تكون هناك نباتات. والحيوانات التي لا تحتوي على الجليكوجين واللاكتوز والكيتين ستواجه صعوبة في ذلك.
دعونا ننظر بعناية في السناجب. الطبيعة هي أعظم سيد الفسيفساء والألغاز: من 20 حمضًا أمينيًا فقط، يتم تشكيل 5 ملايين نوع من البروتينات في جسم الإنسان. تحتوي السناجب أيضًا على الكثير من الحياة وظائف مهمة. على سبيل المثال، البناء، وتنظيم العمليات في الجسم، وتجلط الدم (هناك بروتينات منفصلة لهذا)، والحركة، ونقل بعض المواد في الجسم، فهي أيضًا مصدر للطاقة، في شكل إنزيمات تعمل بمثابة محفز لردود الفعل، وتوفير الحماية. في حماية الجسم من السلبية تأثيرات خارجيةتلعب الأجسام المضادة دورًا مهمًا. وإذا في الكون المثالىيصبح الجسم غير منظم، وبدلاً من تدمير الأعداء الخارجيين، يمكن للأجسام المضادة أن تعمل كمعتدين على أعضاء الجسم وأنسجته.

تنقسم البروتينات أيضًا إلى بسيطة (بروتينات) ومعقدة (بروتينات). ولها خصائص فريدة بالنسبة لها: تمسخ الطبيعة (التدمير، الذي لاحظته أكثر من مرة عند سلق البيضة بشدة) وإعادة الطبيعة (تم العثور على هذه الخاصية تطبيق واسعفي إنتاج المضادات الحيوية والمركزات الغذائية وما إلى ذلك).
دعونا لا نتجاهل الدهون(الدهون). في أجسامنا بمثابة مصدر احتياطي للطاقة. كمذيبات فإنها تساعد على حدوث التفاعلات الكيميائية الحيوية. المشاركة في بناء الجسم - على سبيل المثال، في تكوين أغشية الخلايا.
وبضع كلمات أخرى حول المركبات العضوية المثيرة للاهتمام مثل الهرمونات. يشاركون في التفاعلات الكيميائية الحيوية والتمثيل الغذائي. صغيرة جدًا، الهرمونات تجعل الرجال رجالًا (التستوستيرون) والنساء نساء (الإستروجين). تجعلنا سعداء أو حزينين (تلعب الهرمونات دورًا مهمًا في تقلب المزاج الغدة الدرقية، والإندورفين يعطي الشعور بالسعادة). بل إنهم يحددون ما إذا كنا "بومة ليلية" أو "قبرات". هل أنت مستعد للدراسة في وقت متأخر أو تفضل الاستيقاظ مبكرا والقيام بذلك العمل في المنزللا يتم تحديد ما قبل الذهاب إلى المدرسة من خلال روتينك اليومي فحسب، بل أيضًا من خلال بعض هرمونات الغدة الكظرية.
خاتمة
إن عالم المواد العضوية مدهش حقًا. يكفي أن تتعمق في دراستها قليلاً لتلتقط أنفاسك بعيدًا عن الشعور بالقرابة مع كل أشكال الحياة على الأرض. ساقان أو أربعة أو جذور بدلاً من الأرجل - نحن جميعًا متحدون بسحر المختبر الكيميائي للطبيعة الأم. فهو يتسبب في اتحاد ذرات الكربون معًا في سلاسل، والتفاعل وتكوين الآلاف من المركبات الكيميائية المختلفة.
الآن لديك دليل سريع للكيمياء العضوية. وبطبيعة الحال، لم يتم عرض كافة المعلومات الممكنة هنا. ربما يتعين عليك توضيح بعض النقاط بنفسك. ولكن يمكنك دائمًا استخدام المسار الذي حددناه لأبحاثك المستقلة.
يمكنك أيضًا استخدام تعريف المادة العضوية والتصنيف والصيغ العامة للمركبات العضوية الواردة في المقالة و معلومات عامةعنهم للتحضير لدروس الكيمياء في المدرسة.
أخبرنا في التعليقات ما هو قسم الكيمياء (العضوي أو غير العضوي) الذي تفضله أكثر ولماذا. لا تنسى مشاركة المقال على في الشبكات الاجتماعية، حتى يتمكن زملائك في الفصل من استخدامه أيضًا.
يرجى إعلامي إذا وجدت أي عدم دقة أو أخطاء في المقالة. نحن جميعا بشر وجميعنا نخطئ في بعض الأحيان.
موقع الويب، عند نسخ المادة كليًا أو جزئيًا، يلزم وجود رابط للمصدر.








